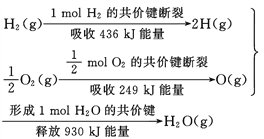
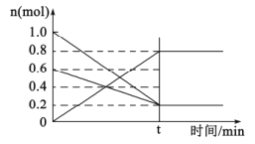
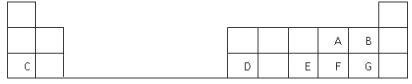
题目内容
【题目】实验测定含有少量氯化钠的碳酸氢钠的含量,完成下列填空:
方案1:取样品溶解后,加试剂使HCO3-沉淀,测定沉淀的质量。
操作步骤有:①称量并溶解样品;②加入足量的Ba(OH)2溶液;③过滤;④洗涤;⑤干燥;⑥称量并进行恒重操作。
(1)实验时所需的定量实验仪器为___,判断是否达到恒重的标准是__。
方案2:用0.100mol/L盐酸滴定。具体过程如图:
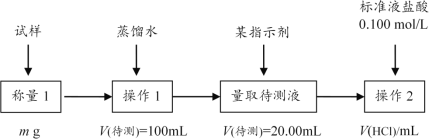
(2)操作1所需要的仪器有__。
(3)操作2时选择的指示剂为甲基橙,当溶液___时,说明达到了操作2终点。为减少实验的偶然误差,通常的处理办法是__。
(4)操作2时若锥形瓶内有少量液体溅出,则测定结果__;若盛装待测液的锥形瓶未用待测液润洗,测定结果___。(选填“偏高”、“偏低”或“无影响”)
(5)用图中的数据,计算小苏打中碳酸氢钠的质量分数___。
方案3:用稀盐酸将HCO3-转化为CO2,测定CO2的体积。
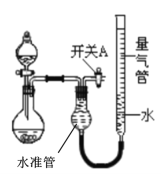
(6)为保证读数的准确性并易于观察,实验中量气管中的液体最好是__(填字母编号)。
a.饱和碳酸钠溶液 b.饱和碳酸氢钠溶液 c.含有品红的硫酸溶液
本实验应对量气管多次读数,读数时应注意:
①将实验装置恢复到室温,
②___,
③视线与凹液面最低处相平。
【答案】电子天平 前后两次称量的质量差不超过0.001g 烧杯、玻璃棒、100mL容量瓶、胶头滴管 黄色恰好变成橙色,且半分钟内不褪色 做2~3次平行实验,取平均值 偏低 无影响 ![]() c 调节量气管和水准管液面相平
c 调节量气管和水准管液面相平
【解析】
(1) 方案一根据天平的感量确定称量仪器,当前后两次称量的质量差不超过0.001 g时说明
已经达到恒重;
(2)根据一定物质的量浓度溶液的配制步骤选取实验仪器;
(3)甲基橙的变色范围是3.1-4.4,碳酸钠溶液呈碱性,所以滴有甲基橙的碳酸钠溶液呈黄色,当滴定终点时,溶液黄色恰好变成橙色;为减少误差,应多做几次实验取平均值;
(4)能影响溶质物质的量的因素影响测定结果,否则不影响测定结果;
(5)写出离子方程式或化学方程式,根据物质间存在的量的关系即可求出碳酸氢钠的物质的量,进而求出其质量,将其比上样品的质量可求出碳酸氢钠的质量分数;
(6)对于读数,为了使读书结果较精准,一般应注意:①将实验装置恢复到室温 ②视线与凹液面最低处相平。题目中还要调节量气管和水准管液面相平。
(1) 方案一托盘天平的感量是0.1g,电子天平的感量是0.001g,所以称量药品时用电子天平,当前后两次称量的质量差不超过0.001 g时说明已经达到恒重;
(2)配制一定物质的量浓度溶液时,用烧杯溶解固体药品,用玻璃棒搅拌固体溶解和引流溶液,用容量瓶配制溶液,用胶头滴管定容;
(3)甲基橙的变色范围是3.1~4.4,碳酸钠溶液呈碱性,所以滴有甲基橙的碳酸钠溶液呈黄色,当滴定终点时,溶液呈酸性,溶液黄色恰好变成橙色,且半分钟内不褪色;为减少误差,应多做几次实验取平均值,即做2~3次平行实验;
(4)滴定时若锥形瓶内有少量液体溅出,导致锥形瓶内溶液中溶质减少,所以测定结果偏低,若盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗,对锥形瓶内溶液中的溶质无影响,所以对结果无影响;
(5)滴定20.00mL的待测液消耗的0.1mol/L的盐酸溶液为V mL,则消耗的n(H+)=n(HCl)=V×10-4 mol,根据离子方程式:H++HCO3-=H2O+CO2↑,可知n(HCO3-)=n(H+)=n(HCl)= V×10-4 mol,又取了m g的样品配成了100 mL溶液,测定时只取了20mL,所以小苏打中碳酸氢钠的质量分数为: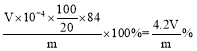 ;
;
(6)a.饱和碳酸钠溶液会与二氧化碳反应,导致实验存在较大误差,a不符合;
b.盐酸具有挥发性,若量器管中液体为饱和碳酸氢钠溶液,则挥发出来的HCl会与之反应产生二氧化碳,使得实验结果偏大,b不符合题意;
c.含有品红的硫酸溶液呈现红色,便于读数,且二氧化碳为酸性气体,几乎不溶于硫酸溶液中,使得实验结果更精确,c符合题意;由于气体的体积受温度和压强影响大,读数时应注意:①将实验装置恢复到室温 ②调节量气管和水准管液面相平 ③视线与凹液面最低处相平。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】合成氨技术的创立开辟了人工固氮的重要途径,其研究来自正确的理论指导,合成氨反应的平衡常数K值和温度的关系如下:
温 度(℃) | 360 | 440 | 520 |
K值 | 0.036 | 0.010 | 0.0038 |
(1)①由上表数据可知该反应为______ (填“放热”,“吸热”,“无法确定”)反应。
②下列措施能用勒夏特列原理解释是__________。(填序号)
A.增大压强有利于合成氨
B.使用合适的催化剂有利于快速生成氨
C.生产中需要升高温度至500C左右
D.需要使用过量的N2,提高H2转化率
(2)常温时,将amol氨气溶于水后,再通入bmol氯化氢,溶液体积为1L,且c(NH4+)=c(Cl),则一水合氨的电离平衡常数Kb=_______________。(用ab表示)
(3)原料气H2可通过反应 CH4(g) + H2O (g)![]() CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的
CO(g) + 3H2(g) 获取,已知该反应中,当初始混合气中的![]() 恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:
恒定时,温度、压强对平衡混合气CH4含量的影响如图所示:

①图中,两条曲线所表示压强的关系是:P1__________P2(填“>”、“=”或“<”)。
②其它条件一定,升高温度,氢气的产率会__________。(填“增大”,“减小”,“不变”)
(4)原料气H2还可通过反应CO(g) + H2O(g) ![]() CO2 (g) + H2(g) 获取。
CO2 (g) + H2(g) 获取。
①T ℃时,向容积固定为5L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08 mol·L-1,该温度下反应的平衡常数K值为______________。
②保持温度仍为T ℃,容积体积为5L,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的_____(填序号)。
A.容器内压强不随时间改变
B.混合气体的密度不随时间改变
C.单位时间内生成a mol CO2的同时消耗a mol H2
D.混合气中n(CO) : n(H2O) : n(CO2) : n(H2) = 1 : 16 : 6 : 6
【题目】实验小组同学探究稀H2SO4对溶液中的I—被O2 氧化的影响因素。
(1)为了探究c(H+)对反应速率的影响,进行实验:
10mL 1mol· L-1 KI溶液5滴淀粉溶液 | 序号 | 加入试剂 | 变色时间 |
Ⅰ | 10mL蒸馏水 | 长时间放置,未见明显变化 | |
Ⅱ | 10mL 0.1mol· L-1H2SO4溶液 | 放置3min后,溶液变蓝 | |
Ⅲ | 10mL 0.2mol· L-1H2SO4溶液 | 放置1min后,溶液变蓝 | |
Ⅳ | 10mL 0.1mol· L-1K2SO4溶液 | 长时间放置,未见明显变化 |
① 写出实验Ⅱ发生反应的离子方程式 ______。
② 实验Ⅰ~Ⅲ所得结论:_______。
③ 增大实验Ⅱ反应速率还可以采取的措施 ______。
④ 实验Ⅳ的作用是______。
(2)为探究c(H+)除了对反应速率影响外,是否还有其他影响,提出假设:
ⅰ. 增大c(H+),增强O2的氧化性;
ⅱ. 增大c(H+),_______。
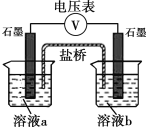
小组同学利用下图装置设计实验方案,对假设进行验证。
| 序号 | 溶液a | 溶液b | 现象 |
Ⅴ | 10mL 1mol· L-1 KI溶液 10mL H2O | 10mL 0.1mol·L-1K2SO4溶液 10mLH2O | 指针未见偏转 | |
Ⅵ | 10mL 1mol· L-1 KI溶液 10mL H2O | 10mL 0.1mol·L-1K2SO4溶液 1mL 0.2mol·L-1H2SO4溶液 9mL H2O | 指针 偏转 | |
Ⅶ | X | 10mL 0.1mol·L-1K2SO4溶液 10mL 0.2mol·L-1H2SO4溶液 | Y | |
Ⅷ | Z | 10mL 0.1mol·L-1K2SO4溶液 10mLH2O | 指针未见偏转 |
通过实验证实假设ⅰ合理,将表中空白处的试剂或现象补充完整。
X __________;Y _________;Z __________。