题目内容
1.实验室里用下列仪器和药品来制取纯净的无水氯化铜:| 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 仪器及装置图 |  | 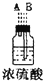 | 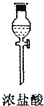 | 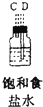 | 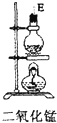 | 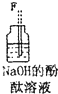 |
(1)如果所制气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)③接⑤接④接②接①接⑥.
(2)实验开始时,应首先检查该装置的检验装置气密性;实验结束时,应先熄灭①处的酒精灯.
(3)待充分反应后,装置①的玻璃管中剩余物呈棕黄色.冷却后,将制得的产物配成饱和溶液,溶液呈绿(或蓝绿)色.
(4)装置④的作用是除去氯气中的氯化氢;装置⑥中的现象是红色逐渐褪去,发生反应的离子方程式是Cl2+2OH-=Cl-+ClO-+H2O.
分析 (1)仪器的连接方法:先制备反应物,然后除杂质,再使氯气与铜反应,最后尾气处理;进行气体除杂或者干燥时,连接顺序一般是:“长进短出”的原则,根据题中实验原理,用浓盐酸与二氧化锰反生成氯气,除杂后与铜反应生成氯化铜,尾气用氢氧化钠吸收,据此答题;
(2)实验中涉及气体的,实验开始时一般都要检验装置气密性,为了防止空气中的成分的干扰,实验结束时,有铜粉的装置中还应再能一会儿氯气;
(3)氯化铜固体为棕黄色,氯化铜饱和溶液呈绿色(或蓝绿色);
(4)饱和食盐水可以除去氯气中的氯化氢,氢氧化钠的酚酞溶液呈红色,吸收多余的氯气溶液碱性减弱,据此判断颜色变化,氯气与氢氧化钠反应生成氯化钠和次氯酸钠,根据电荷守恒书写离子方程式;
解答 解:(1)仪器的连接方法:先制备反应物,然后除杂质,再使氯气与铜反应,最后尾气处理;进行气体除杂或者干燥时,连接顺序一般是:“长进短出”的原则,根据题中实验原理,用浓盐酸与二氧化锰反生成氯气,除杂后与铜反应生成氯化铜,尾气用氢氧化钠吸收,所以仪器连接顺序为:③⑤④②①⑥,
故答案为:③⑤④②①⑥;
(2)实验中涉及气体的,实验开始时一般都要检验装置气密性,为了防止空气中的成分的干扰,实验结束时,有铜粉的装置中还应再能一会儿氯气,所以实验结束时,应先熄灭①处的酒精灯,
故答案为:检验装置气密性;①;
(3)氯化铜固体为棕黄色,氯化铜饱和溶液呈绿色(或蓝绿色),所以装置①的玻璃管中剩余物呈棕黄色,冷却后,将制得的产物配成饱和溶液,溶液呈绿色(或蓝绿色),
故答案为:棕黄;绿(或蓝绿);
(4)饱和食盐水可以除去氯气中的氯化氢,氢氧化钠的酚酞溶液呈红色,吸收多余的氯气溶液碱性减弱,所以装置⑥中的现象是红色逐渐褪去,氯气与氢氧化钠反应生成氯化钠和次氯酸钠,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O,
故答案为:除去氯气中的氯化氢;红色逐渐褪去;Cl2+2OH-=Cl-+ClO-+H2O.
点评 本题考查了常见气体的制取和收集及实验的注意事项,氯化铁的性质和制取;关键是掌握其选择的依据及原理,在装置的分析中明确装置的特点及其作用,难度较大.

| A. | H2O、H2S、H2Se | B. | Hg、Na、NaCl | ||
| C. | 晶体硅、金刚石、碳化硅 | D. | S、Br2、O3 |
| A. | 明矾常作为消毒剂 | |
| B. | 水晶项链和餐桌上的瓷盘都是硅酸盐制品 | |
| C. | 高纯度的硅单质广泛用于制作光导纤维 | |
| D. | 钠的还原性很强,可以用来冶炼金属钛、钽、铌、锆等 |
(1)利用反应Ca(s)+O2$\frac{\underline{\;\;△\;\;}}{\;}$CaO2(s),在纯氧条件下,制取CaO2的装置示意图1如下:
请回答下列问题:
①装置A中反应的化学方程式为2H2O2$\frac{\underline{\;MnO_{2}\;}}{\;}$2H2O+O2↑;仪器a的名称为蒸馏烧瓶;
装置D中盛有的液体是浓硫酸,其作用一是观察氧气的流速,判断氧气通入是否过快及氧气与钙反应进行的程度;二是防止空气进入C装置影响产品纯度.仪器安装后应进行的实验操作:
a.通入氧气 b.检查装置气密性 c.加入药品 d.停止通氧气
e.点燃酒精灯 f.熄灭酒精灯 g.冷却至室温,
正确的操作顺序为bcaefgd.
②完全反应后,有关数据记录如下:
| 空瓷舟质量m0/g | 瓷舟与钙的质量m1/g | 瓷舟与产物的质量m2/g |
| 14.80 | 15.08 | 15.25 |
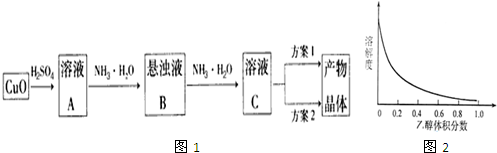
(2)利用反应Ca2++H2O2+2NH3•H2O+6H2O=CaO2•8H2O+2NH4+,在碱性环境中,制取CaO2的流程示意图2如下:
请回答下列问题:
①主反应中,NH3•H2O在Ca2+和H2O2的反应历程中所起的作用是中和过氧化氢和Ca2+反应析出的氢离子,促进反应进行;该反应所需的条件及操作为acf(填字母).
a.把氯化钙溶液逐滴加入过氧化氢-氨水溶液中
b.把过氧化氢-氨水溶液逐滴加入氯化钙溶液中
c.滴加时先搅拌后静置,观察晶体析出
d.滴加时不停搅拌,直至晶体完全析出
e.反应体系热水浴加热
f.反应体系冰水浴冷却
洗涤CaO2•8H2O晶体时,判断晶体是否完全洗净的试剂为AgNO3溶液;滤液循环使用时需在反应器中加入一种物质,该物质的化学式为Ca(OH)2.
②利用反应2CaO2 >350℃?2CaO+O2↑测量产品中CaO2含量时,停止反应且冷却至25℃后的装置示意图3如下:若直接读数确定25℃、1大气压下气体的体积,则测量结果偏大(填“偏大”、“偏小”或“无影响”).

| A. | 石墨不如金刚石稳定 | |
| B. | 金刚石与石墨一样稳定 | |
| C. | 等质量的金刚石与石墨完全燃烧,放出的能量一样多 | |
| D. | 等质量的金刚石与石墨完全燃烧,石墨放出的能量少 |
| A. | 强酸跟强碱反应放出的热量一定是中和热 | |
| B. | 1 mol酸与1 mol碱完全反应放出的热量是中和热 | |
| C. | 在稀溶液中,强酸与强碱发生中和反应生成1 mol H2O(l)时的反应热叫做中和热 | |
| D. | 表示中和热的离子方程式为H++OH-═H2O△H=-57.3 kJ/mol |
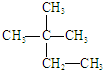 ③氧气 ④氯气 ⑤
③氧气 ④氯气 ⑤ ⑥${\;}_{17}^{37}$Cl ⑦${\;}_{17}^{35}$Cl ⑧臭氧.
⑥${\;}_{17}^{37}$Cl ⑦${\;}_{17}^{35}$Cl ⑧臭氧.