题目内容
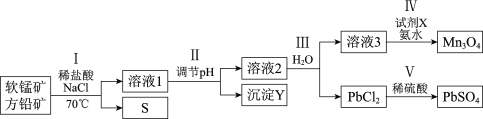
【题目】工业上应用两矿法浸出软锰矿(主要成分MnO2)和方铅矿(主要成分PbS、FeS2),制备PbSO4和Mn3O4,转化流程如下。
已知:PbCl2微溶于水,溶液中存在可逆反应:![]() 。
。
下列说法正确的是
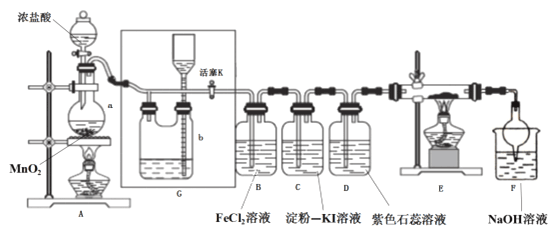
A.Ⅰ中可使用浓盐酸代替稀盐酸和NaCl的混合溶液
B.Ⅱ中生成的沉淀Y是Fe(OH)2
C.Ⅳ中试剂X可能作氧化剂
D.Ⅴ中发生反应:Pb2++SO42-== PbSO4
【答案】C
【解析】
方铅矿 (主要成分PbS、、FeS2)和软锰矿(主要成分MnO2)中加入稀盐酸、NaCl溶液并加热至70℃,发生的反应有MnO2+PbS+4HCl=MnCl2+PbCl2+S+ 2H2O,3MnO2+2FeS2+12HCl=3MnCl2+2FeCl3+4S+6H2O,调节溶液的pH使铁离子和转化为沉淀,要除去这两种离子需要加入碱性物质且不能引进新的杂质,然后过滤得到氢氧化铁沉淀和滤液,将溶液蒸发浓缩、冷却结晶、过滤得到PbCl2晶体和滤液,向滤液中通入氨气、X使锰离子被氧化生成Mn3O4,将溶液过滤得到Mn3O4和滤液,据此解答。
A.若用浓盐酸代替稀盐酸和NaCl的混合溶液,那么浓盐酸与软锰矿中的MnO2反应生成氯气,A错误;
B.由分析可知Ⅱ中生成的沉淀Y是Fe(OH)3,B错误;
C.Ⅳ中向滤液中通入氨气、X使锰离子被氧化生成Mn3O4,则试剂X可能作氧化剂,C正确;
D.因为PbCl2微溶于水,溶液中存在可逆反应:![]() ,故Ⅴ中发生反应:PbCl42-+SO42-== PbSO4+4Cl-,D错误;
,故Ⅴ中发生反应:PbCl42-+SO42-== PbSO4+4Cl-,D错误;
故选C。

练习册系列答案
相关题目