题目内容
【题目】天然气部分氧化制取的化工原料气中,常含有氧硫化碳(COS,结构类似于CO2),目前氧硫化碳脱除可采用氢解和水解两种方法,其反应原理如下:
氢解:COS(g)+H2(g)![]() H2S(g)+CO(g)
H2S(g)+CO(g)
水解:COS(g)+H2O(g)![]() H2S(g)+CO2(g)
H2S(g)+CO2(g)
(1)氧硫化碳的电子式为________________________________。
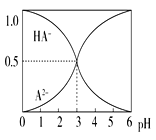
(2)如下图是氧硫化碳水解和氢解平衡转化率随温度变化曲线。
①观察图像,水解与氢解相比优势为_________________________________。
②水解的△H___0(填“大于"或“小于”)
③已知:1molCOS(g)完全氢解能量变化为6.99kJ,若初始COS的物质的量为nmol,从反应开始到R点所示体系的能量变化为______kJ(只列式,不必计算)。

(3)氢解和水解产生的H2S必须进行回收处理,酸性、可溶性铁盐氧化H2S制取硫磺工艺备受重视。
①写出酸性条件下用氢氧化铁溶液吸收H2S制取硫磺的离子方程式___________________________。
②吸收H2S后的酸性废液中的Fe2+,可通过电解法使Fe3+再生,写出电解时总反应的离子方程式:__________。
③常温下,在c(H+)=0.30mo/L的酸性溶液中通入H2S至饱和,测得硫化氢的平衡浓度为0.10mol/L,计算此时溶液中c(S2-)=_______[忽略H2S电离生成的H+,Ka1(H2S)=1.3×10-7,Ka2(H2S)=7.0×10-15,结果保留两位有效数字。]
【答案】 ![]() 水解利用廉价水蒸气作转化剂,比氢气便宜、易得(或水解在较低温度下,氧硫化碳具有较高的转化率,比氢解节约能源) 小于 96%n×6.99 2Fe3++H2S=2Fe2++2H++S Fe2++2H+
水解利用廉价水蒸气作转化剂,比氢气便宜、易得(或水解在较低温度下,氧硫化碳具有较高的转化率,比氢解节约能源) 小于 96%n×6.99 2Fe3++H2S=2Fe2++2H++S Fe2++2H+![]() 2Fe3++H2↑ 1.0×10-21mol/L
2Fe3++H2↑ 1.0×10-21mol/L
【解析】(1)氧硫化碳的电子式为![]() ;(2)①观察图像,根据氧硫化碳水解和氢解平衡转化率随温度变化曲线可知,水解与氢解相比优势为:水解利用廉价水蒸气作转化剂,比氢气便宜、易得(或水解在较低温度下,氧硫化碳具有较高的转化率,比氢解节约能源);②根据曲线变化可知,升高温度,水解的平衡转化率降低,平衡逆向移动,逆反应为吸热,正反应为放热,△H小于0;③已知:1molCOS(g)完全氢解能量变化为6.99kJ,若初始COS的物质的量为nmol,从反应开始到R点(转化率为96%)所示体系的能量变化为96%×nmol×6.99kJ =96%n×6.99kJ;(3)①酸性条件下用氢氧化铁溶液吸收H2S制取硫磺,同时产生Fe2+,反应的离子方程式2Fe3++H2S=2Fe2++2H++S;②吸收H2S后的酸性废液中的Fe2+,可通过电解法使Fe3+再生,电解时Fe2+失电子产生Fe3+,H+得电子产生H2,故总反应的离子方程式:Fe2++2H+
;(2)①观察图像,根据氧硫化碳水解和氢解平衡转化率随温度变化曲线可知,水解与氢解相比优势为:水解利用廉价水蒸气作转化剂,比氢气便宜、易得(或水解在较低温度下,氧硫化碳具有较高的转化率,比氢解节约能源);②根据曲线变化可知,升高温度,水解的平衡转化率降低,平衡逆向移动,逆反应为吸热,正反应为放热,△H小于0;③已知:1molCOS(g)完全氢解能量变化为6.99kJ,若初始COS的物质的量为nmol,从反应开始到R点(转化率为96%)所示体系的能量变化为96%×nmol×6.99kJ =96%n×6.99kJ;(3)①酸性条件下用氢氧化铁溶液吸收H2S制取硫磺,同时产生Fe2+,反应的离子方程式2Fe3++H2S=2Fe2++2H++S;②吸收H2S后的酸性废液中的Fe2+,可通过电解法使Fe3+再生,电解时Fe2+失电子产生Fe3+,H+得电子产生H2,故总反应的离子方程式:Fe2++2H+![]() 2Fe3++H2↑;
2Fe3++H2↑;
③ H2S ![]() H+ + HS-
H+ + HS-
0.1mol/L 0.30ml/L c(HS-)
则Ka1(H2S)=  =
=![]() =1.3×10-7,解得c(HS-)=4.3×10-8mol/L;
=1.3×10-7,解得c(HS-)=4.3×10-8mol/L;
HS- ![]() H+ + S2-
H+ + S2-
4.3×10-8mol/L 0.30ml/L c(S2-)
则Ka2(H2S)=  =
=![]() =7.0×10-15,解得c(S2-)=1.0×10-21mol/L。
=7.0×10-15,解得c(S2-)=1.0×10-21mol/L。