题目内容
(12分)熟悉和使用中学化学实验中常见仪器及用品,是化学学习的基本要求。试回答以下问题:
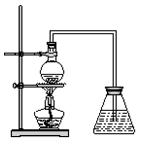
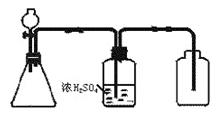
(1)用装置甲、乙、丙和乳胶管组成一套装置(气密性已检查),可用于制取并收集NH3或HCl气体。可供选择的液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。请回答下列问题:

①若制取某气体的过程中,丙中的石蕊溶液变红,且烧瓶中的试剂A与分液漏斗中的试剂B为无色液体,则试剂A为_________,制取该气体利用了B的性质有_______、______________。
通过丙中紫色石蕊溶液变红或变蓝,说明乙中气体已集满。若石蕊溶液变蓝,则烧瓶中应加入的固体试剂A为_______________________。
②若在乙中收集氨气,气体流经装置的顺序是:a→______→_____→d(填接口代号)
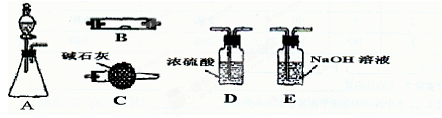
(2)下图中的装置D是实验室制备CO2的简易装置图,用该装置制备CO2可起到随时使反应发生,也可以随时使反应停止的效果。下图中的装置A、B、C也可起到相同效果的有__________(填写编号)。
(1)用装置甲、乙、丙和乳胶管组成一套装置(气密性已检查),可用于制取并收集NH3或HCl气体。可供选择的液体试剂有:浓硫酸、浓盐酸、浓氨水,丙中试剂为紫色石蕊溶液。请回答下列问题:

①若制取某气体的过程中,丙中的石蕊溶液变红,且烧瓶中的试剂A与分液漏斗中的试剂B为无色液体,则试剂A为_________,制取该气体利用了B的性质有_______、______________。
通过丙中紫色石蕊溶液变红或变蓝,说明乙中气体已集满。若石蕊溶液变蓝,则烧瓶中应加入的固体试剂A为_______________________。
②若在乙中收集氨气,气体流经装置的顺序是:a→______→_____→d(填接口代号)
(2)下图中的装置D是实验室制备CO2的简易装置图,用该装置制备CO2可起到随时使反应发生,也可以随时使反应停止的效果。下图中的装置A、B、C也可起到相同效果的有__________(填写编号)。

(1)①浓盐酸 吸水性 溶于水放出大量的热 NaOH或CaO或碱石灰 ②c b
(2)B
(2)B
略

练习册系列答案
相关题目
 %的浓硫酸(ρ= 1.84g/cm3)配制浓度为0.5 mol/L的稀硫酸500mL。有以下几步操作,请按要求回答下列问题:
%的浓硫酸(ρ= 1.84g/cm3)配制浓度为0.5 mol/L的稀硫酸500mL。有以下几步操作,请按要求回答下列问题:  。
。 CaCl2 + 2NH3↑+ 2H2O
CaCl2 + 2NH3↑+ 2H2O
 气泄漏事件,500 多居民深夜大转移。假如你在现场,你会采用什么自救为法? 。
气泄漏事件,500 多居民深夜大转移。假如你在现场,你会采用什么自救为法? 。

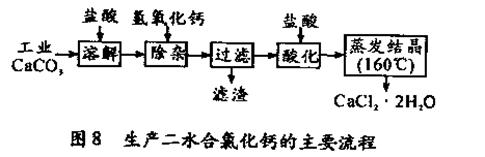
 。
。 。
。
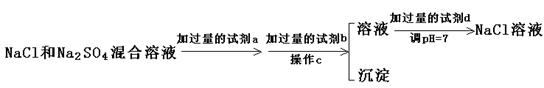
 。
。