题目内容
13.若乙酸分子中的羟基“-OH”用18O标记,将之与乙醇反应,二者在浓H2SO4作用下发生反应,一段时间后,分子中含有18O的物质有( )| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
分析 乙酸与乙醇反应,乙酸中的羧基提供羟基,乙醇中的羟基提供氢原子,羟基和氢原子形成水,剩下基团结合的形成酯,据此进行判断.
解答 解:乙酸与乙醇反应,乙酸中的羧基提供羟基,乙醇中的羟基提供氢原子,羟基和氢原子形成水,剩下基团结合的形成酯:CH3C16O18OH+CH3CH216OH?CH3C16O16OC2H5+H218O,所以分子中含有18O的物质总共有2种,分别为:CH3C16O18OH、H218O,
故选B.
点评 本题考查羧酸与醇反应的原理,题目难度不大,注意明确酯化反应原理:“酸脱羟基醇脱氢”即 乙酸中的羧基提供羟基,乙醇中的羟基提供氢原子.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
4.热化学方程式2H2(g)+O2(g)═2H2O(g)△H=-483.6 kJ•mol-1中,化学式前面的化学计量数表示( )
| A. | 分子数 | B. | 体积 | C. | 质量 | D. | 物质的量 |
1.下列表述Ⅰ、表述Ⅱ均正确,且没有因果关系的是( )
| 表述Ⅰ | 表述Ⅱ | |
| A | 在水中,NH3溶解度比I2的溶解度大 | NH3是极性分子,I2是非极性分子 |
| B | 通常条件下,HCl比HI稳定性高 | 非金属性:Cl>I |
| C | NH2OH中N的化合价为:-3 | 电负性:Cl>N |
| D | 沸点:SiO2>CO2 | 式量:SiO2>CO2 |
| A. | A | B. | B | C. | C | D. | D |
18.下列物质的制备方法恰当的是( )
| A. | 往95%酒精中加入无水氯化钙,蒸馏得到无水乙醇 | |
| B. | 往2mL 10% CuSO4 溶液中滴加几滴2% NaOH,然后滴加少量乙醛,加热制得砖红色沉淀Cu2O | |
| C. | 用氯气和乙烷按1:1体积比混合,光照条件下,制纯一氯乙烷 | |
| D. | 往装有电石的烧瓶中逐滴滴加饱和食盐水,制粗乙炔 |
5.下列各组中的性质比较,正确的是( )
| A. | 稳定性:NH3<PH3<SiH4 | B. | 酸性:HClO>H2SO3>H3PO4 | ||
| C. | 碱性:KOH>NaOH>Mg(OH)2 | D. | 还原性:F->Cl->Br->I- |
3.下列有关胶体的说法不正确的是( )
| A. | 电泳现象可证明胶体带有电荷 | |
| B. | 分散质粒子直径介于10-9 m~10-7m之间的分散系称为胶体 | |
| C. | 向Fe(OH)3胶体中滴入少量稀H2SO4,有红褐色沉淀产生 | |
| D. | 放电影时,放映室射到银幕上的光柱的形成属于丁达尔效应 |
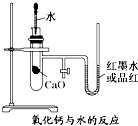 如图是某同学设计的放热反应的观察装置.
如图是某同学设计的放热反应的观察装置.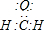 .
.