题目内容
【题目】下列有关物质的用途错误的是( )
A.水玻璃用作木材防火剂
B.高纯度的硅是制造光导纤维的材料
C.可用氢氟酸刻蚀玻璃
D.氢氧化铝、小苏打可用于治疗胃酸过多症
【答案】B
【解析】解:A.硅酸钠的水溶液是水玻璃,硅酸钠不燃烧也不支持燃烧,所以水玻璃可用作木材防火剂,故A正确;B.二氧化硅是制造光导纤维的材料,是利用光的全反射原理,故B错误;
C.氢氟酸与二氧化硅反应,可用于刻蚀玻璃,故C正确;
D.小苏打、氢氧化铝它们的水溶液呈碱性,胃酸的主要成分为盐酸,故都能发生复分解反应,可用于治疗胃酸过多,故D正确;
故选B.

【题目】常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料。某探究小组利用下列反应和装置制备一硝基甲苯。
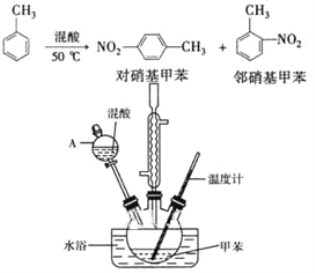
实验中可能用到的数据:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:①按体积比1:3配制浓硫酸与浓硝酸混合物40 mL;
②在三颈瓶中加入15 mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10 min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60 g。
请回答下列问题:
(1)配制混酸的方法是_______________________。反应中需不断搅拌,目的是__________________________________________。
(2)仪器A的名称是______,使用该仪器前必须进行的操作是____。
(3)若实验后在三颈瓶中收集到的产物较少,可能的原因是_____。
(4)分离反应后产物的方案如下:

其中,操作1的名称为______,操作2中需要使用下列仪器中的____(填序号)。
a.冷凝管 b.酒精灯 c.温度计 d.分液漏斗 e.蒸发皿
(5)该实验中一硝基甲苯的产率为______(保留4位有效数字)。
【题目】煤的主要组成元素是碳、氢、氧、硫、氮,还有极少量的磷、砷、锗、镓、铟等元素,燃煤产生CxHy、SO2等大气污染物,煤的气化是高效、清洁利用煤炭的重要途径之一。回答下列问题:
(1)锗是第四周期第ⅣA族元素,其原子结构示意图为_______________________。
(2)利用煤的气化获得的水煤气(主要成分为CO、CO2和H2)在催化剂作用下可以合成绿色燃料甲醇。
已知:H2O(l)=H2O(g) △H1=+44.0kJ/mol
CO2(g)+H2(g)=CO(g)+H2O(l) △H2=-3.0 kJ/mol
CO2(g)+3H2(g)=CH3OH(g)+H2O(g) △H3=-58.7 kJ/mol
写出由CO 与 H2制备 CH3OH 气体的热化学方程式___________________________________。
(3)甲醇和CO2可直接合成碳酸二甲酯(CH3OCOOCH3,简称DMC) :
2CH3OH(g)+CO2(g)![]() CH3OCOOCH3(g)+H2O(g) ΔH4<0
CH3OCOOCH3(g)+H2O(g) ΔH4<0
①该化学反应的平衡常数表达式为K=_________________________。
②在恒温恒容密闭容器中发生上述反应,能说明反应达到平衡状态的是_____________(填标号)。
A.v正(CH3OH)= 2v逆(H2O) B.容器内气体的密度不变
C.容器内压强不变 D.CH3OH与CO2的物质的量之比保持不变
③一定条件下分别向甲、乙丙个恒容密团容器中加入一定量的初始物质发生该反应,各容器中温度、反应物的起始量如下表,反应过程中DMC的物质的量依度随时间变化如下图所示:
容器 | 甲 | 乙 | 丙 |
容积(L) | 0.5 | 0.5 | V |
温度(℃) | T1 | T2 | T1 |
起始量 | 1molCO2(g)2molCH3OH(g) | 1molDMC(g)1mol H2O (g) | 2molCO2(g)2molCH3OH(g) |
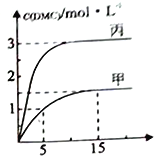
甲容器中,在5-15min中的平均反应速率v(CO2) =_____________。乙容器中,若平衡时n(CO2) =0.2mol,则T1________T2(填“>”“<"或”=”)。甲、丙两容器的反应达平衡时CO2的转化率:甲________丙(填“>”“<"或”=”)。
(4)一定温度下,用水吸收SO2气体时,溶液中水的电离平衡_________移动(填“向左” “向右”或“不”);若得到pH=4的H2SO3溶液,试计算溶液中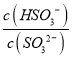 =____________。SO2可用足量小苏打溶液吸收,反应的离子方程式是_________________________________。(已知该温度下,H2SO3的电离常数:K1=4.5×10-2,K2=2.5×10-7,H2CO3的电离常数K1=8.4×10-7,K2=1.2×10-10)
=____________。SO2可用足量小苏打溶液吸收,反应的离子方程式是_________________________________。(已知该温度下,H2SO3的电离常数:K1=4.5×10-2,K2=2.5×10-7,H2CO3的电离常数K1=8.4×10-7,K2=1.2×10-10)