题目内容
【题目】在2 L容积不变的容器中,发生N2+3H2 NH3的反应。现通入4 mol H2和4 mol N2,10 s内用H2表示的反应速率为0.12 mol·L-1·s-1,则10 s后容器中N2的物质的量是( )
A. 1.6 mol B. 2.8 mol C. 3.6 mol D. 3.2 mol
【答案】D
【解析】
v(H2)=0.12mol/(Ls),速率之比等于化学计量数之比,所以v(N2)=![]() v(H2)=
v(H2)=![]() ×0.12mol/(Ls)=0.04mol/(Ls)。所以参加反应N2的物质的量为0.04mol/(Ls)×10s×2L=0.8mol。所以10s后容器中N2的物质的量为4mol-0.8mol=3.2mol。答案选D。
×0.12mol/(Ls)=0.04mol/(Ls)。所以参加反应N2的物质的量为0.04mol/(Ls)×10s×2L=0.8mol。所以10s后容器中N2的物质的量为4mol-0.8mol=3.2mol。答案选D。

练习册系列答案
 捷径训练检测卷系列答案
捷径训练检测卷系列答案 小夫子全能检测系列答案
小夫子全能检测系列答案
相关题目
【题目】某实验兴趣小组按如图装置实验后,所记录内容合理的是
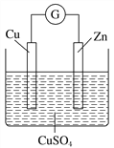
实验记录 | ①Zn片为负极,质量减少,Cu为正极,质量不变; ②外电路电流方向是:由Cu→Zn; ③SO42向Zn极移动,Cu2+向Cu极移动; ④Zn电极发生氧化反应; ⑤正极反应式:Cu2++2e===Cu; ⑥电子流动方向:锌极→导线→铜极→电解质溶液→锌极 |
A. ①②④B. ②③④C. ②③④⑤D. ②③④⑤⑥