题目内容
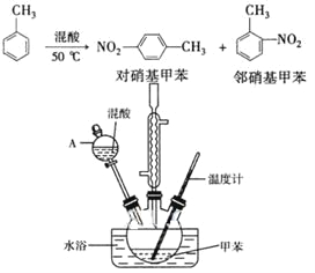
【题目】常见的一硝基甲苯有对硝基甲苯和邻硝基甲苯两种,均可用于合成各种染料。某探究小组利用下列反应和装置制备一硝基甲苯。
实验中可能用到的数据:
密度/g·cm-3 | 沸点/℃ | 溶解性 | |
甲苯 | 0.866 | 110.6 | 不溶于水,易溶于硝基甲苯 |
对硝基甲苯 | 1.286 | 237.7 | 不溶于水,易溶于液态烃 |
邻硝基甲苯 | 1.162 | 222 | 不溶于水,易溶于液态烃 |
实验步骤:①按体积比1:3配制浓硫酸与浓硝酸混合物40 mL;
②在三颈瓶中加入15 mL(13g)甲苯,按图所示装好药品和其他仪器;
③向三颈瓶中加入混酸,并不断搅拌(磁力搅拌器已略去);
④控制温度约为50℃,反应大约10 min,三颈瓶底有大量淡黄色油状液体出现;
⑤分离出一硝基甲苯的总质量13.60 g。
请回答下列问题:
(1)配制混酸的方法是_______________________。反应中需不断搅拌,目的是__________________________________________。
(2)仪器A的名称是______,使用该仪器前必须进行的操作是____。
(3)若实验后在三颈瓶中收集到的产物较少,可能的原因是_____。
(4)分离反应后产物的方案如下:

其中,操作1的名称为______,操作2中需要使用下列仪器中的____(填序号)。
a.冷凝管 b.酒精灯 c.温度计 d.分液漏斗 e.蒸发皿
(5)该实验中一硝基甲苯的产率为______(保留4位有效数字)。
【答案】 分别量取10 mL和30 mL的浓硫酸和浓硝酸,将浓硝酸倒入烧杯中,浓硫酸沿着烧杯内壁缓缓注入,并不断搅拌; 使反应充分进行,并防止温度过高有其他副产物生成 分液漏斗 检查是否漏液 温度过高,导致HNO3大量挥发 分液 abc 70.25%
【解析】⑴. 配制混酸时,分别量取10mL和30mL的浓硫酸和浓硝酸,将浓硝酸倒入烧杯中,浓硫酸沿着烧杯内壁缓缓注入,并不断搅拌,如果将浓硝酸加到浓硫酸中可能发生液体飞溅的情况。搅拌的目的是为了使反应充分进行,并防止温度过高有其他副产物生成;
故答案为:分别量取10mL和30mL的浓硫酸和浓硝酸,将浓硝酸倒入烧杯中,浓硫酸沿着烧杯内壁缓缓注入,并不断搅拌;使反应充分进行,并防止温度过高有其他副产物生成;
⑵. 仪器A是分液漏斗,使用前必须检查是否漏液;故答案为:分液漏斗;检查是否漏液;
⑶. 若实验后在三颈瓶中收集到的产物较少,可能的原因是温度过高,导致HNO3大量挥发,故答案为:温度过高,导致HNO3大量挥发;
⑷. 因为分离得到的是无机和有机两种液体,而有机物和无机物是不相溶的,因此方法是分液;分离两种硝基化合物只能利用它们沸点的不同,因此采用蒸馏的方法,使用到所提供仪器中的分别是:酒精灯、温度计、冷凝管;故答案为:分液;abc;
⑸. 产率的计算方法是用实际产量除以理论产量,根椐方程式,1mol的甲苯可以得到1mol的对硝基甲苯与1mol的邻硝基甲苯,换算成质量应该是:92g的甲苯可以得到137g的对硝基苯和137g的邻硝基苯,则13g的甲苯可得到的一硝基苯的质量是: ![]() =19.35g,所以一硝基苯的产量为:
=19.35g,所以一硝基苯的产量为: ![]() ×100%=70.25%;故答案为:70.25%.
×100%=70.25%;故答案为:70.25%.

【题目】某实验兴趣小组按如图装置实验后,所记录内容合理的是
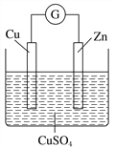
实验记录 | ①Zn片为负极,质量减少,Cu为正极,质量不变; ②外电路电流方向是:由Cu→Zn; ③SO42向Zn极移动,Cu2+向Cu极移动; ④Zn电极发生氧化反应; ⑤正极反应式:Cu2++2e===Cu; ⑥电子流动方向:锌极→导线→铜极→电解质溶液→锌极 |
A. ①②④B. ②③④C. ②③④⑤D. ②③④⑤⑥