题目内容
19.下表为元素周期表前4周期的一部分,且X、Y、Z、R和W为主族元素.下列说法正确的是( )| X | ||
| Y | Z | R |
| W |
| A. | 五种元素的原子最外层电子数一定大于2 | |
| B. | 五种元素一定都是非金属元素 | |
| C. | Z的氧化物与X单质在任何条件下都不会发生置换反应 | |
| D. | R的最外层电子数一定为5 |
分析 图为元素周期表前四周期的一部分,由元素在周期表中的位置可知,应是周期表的2、3、4周期,由于周期表中ⅡA、ⅢA之间相隔10列,且X、Y、Z、R和W均为主族元素,故Y只能为ⅢA族或ⅣA族元素,若Y为ⅢA族,则Y为Al、Z为Si、X为C、R为P、W为Ga;若Y为ⅣA族元素,则Y为Si、Z为P、X为N、R为S、W为Ge,结合元素化合物性质解答.
解答 解:图为元素周期表前四周期的一部分,由元素在周期表中的位置可知,应是周期表的2、3、4周期,由于周期表中ⅡA、ⅢA之间相隔10列,且X、Y、Z、R和W均为主族元素,故Y只能为ⅢA族或ⅣA族元素,若Y为ⅢA族,则Y为Al、Z为Si、X为C、R为P、W为Ga;若Y为ⅣA族元素,则Y为Si、Z为P、X为N、R为S、W为Ge,
A.Y为ⅢA族或ⅣA族元素,其它元素的族序数都大于Y,故5种元素的最外层电子数都大于2,故A正确;
B.根据分析可知,五种元素不可能都是金属元素,故B错误;
C.当Y位于ⅢA族时,X、Z是ⅣA的C、Si,高温下可以发生置换反应:2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑,故C错误;
D.结合分析可知,R的最外层电子数可能为5或6,故D错误;
故选A.
点评 本题考查原子结构与元素周期律的应用,题目难度中等,根据位置关系确定Y所在的族为解答关键,注意熟练掌握原子结构与元素周期律、元素周期表的关系.

练习册系列答案
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案
相关题目
9.有机物A的分子式为C5H12O,且能在铜丝作催化剂和加热的条件下反应,其氧化产物能与新制Cu(OH)2在加热的条件下生成砖红色沉淀,有机物A的结构有(不考虑立体异构)( )
| A. | 2种 | B. | 4种 | C. | 6种 | D. | 8种 |
7.有关物质的分类,下列说法正确的是( )
| A. | CH3CH(CH3)2属于链状化合物 | B. | 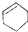 属于芳香族化合物 属于芳香族化合物 | ||
| C. | 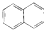 属于脂环化合物 属于脂环化合物 | D. | 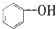 属于芳香烃 属于芳香烃 |
14. 一定温度下,在恒容密闭容器中充入2molNO2与1molO2发生反应如下:4NO2(g)+O2(g)?2N2O5(g)
一定温度下,在恒容密闭容器中充入2molNO2与1molO2发生反应如下:4NO2(g)+O2(g)?2N2O5(g)
(1)已知平衡常数K350℃<K300℃,则该反应是放热反应(填“吸热”或“放热”); 常温下,该反应能逆向自发进行,原因是逆反应方向的△S>0.
(2)下列有关该反应的说法正确的是BD
A.扩大容器体积,平衡向逆反应方向移动,混合气体颜色变深
B.恒温恒容下,再充入2molNO2和1molO2,再次达到平衡时NO2转化率增大
C.恒温恒容下,当容器内的密度不再改变,则反应达到平衡状态
D.若该反应的平衡常数增大,则一定是降低了温度
(3)氮的化合物种类较多,如NH3、NO、NO2、HNO3、硝酸盐等.
①亚硝酸是一种弱酸,能证明亚硝酸是弱电解质的是AD
A.常温下,亚硝酸钠溶液的pH>7
B.亚硝酸能和NaOH发生中和反应
C.用亚硝 酸 溶液做导电性实验,灯泡很暗
D.常温下,将pH=3的亚硝酸溶液稀释10倍,pH<4
②根据酸碱质子理论,凡是能给出质子的分子或离子都是酸,凡是能结合质子的分子或离子都是碱.按照这个理论,下列微粒属于两性物质的是acd
a.H2O b.NO2- c.H2NCH2COOH d.H2PO4- e.H2S
③氮同主族磷元素形成的Na2HPO4溶液显碱性,若向溶液中加入足量的CaCl2溶液,溶液则显酸性,其原因是3Ca2++2HPO42-═Ca3(PO4)2↓+2H+(用离子方程式表示).
(4)X、Y、Z、W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种.下表是常温下浓度均为0.01mol•L-1的X、Y、Z、W溶液的pH.
将X、Y、Z各1mol•L-1同时溶于水中制得混合溶液,则混合溶液中各离子的浓度由大到小的顺序为c(Na+)>c(NO3-)>c(NO2-)>c(OH-)>c(H+).
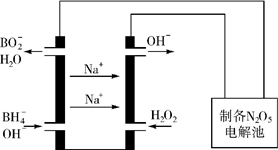
(5)N2O5是一种新型绿色硝化剂,其制备可以用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5,工作原理如图.则硼氢化钠燃料电池的负极反应式为BH4-+8OH--8e-=BO2-+6H2O.
 一定温度下,在恒容密闭容器中充入2molNO2与1molO2发生反应如下:4NO2(g)+O2(g)?2N2O5(g)
一定温度下,在恒容密闭容器中充入2molNO2与1molO2发生反应如下:4NO2(g)+O2(g)?2N2O5(g)(1)已知平衡常数K350℃<K300℃,则该反应是放热反应(填“吸热”或“放热”); 常温下,该反应能逆向自发进行,原因是逆反应方向的△S>0.
(2)下列有关该反应的说法正确的是BD
A.扩大容器体积,平衡向逆反应方向移动,混合气体颜色变深
B.恒温恒容下,再充入2molNO2和1molO2,再次达到平衡时NO2转化率增大
C.恒温恒容下,当容器内的密度不再改变,则反应达到平衡状态
D.若该反应的平衡常数增大,则一定是降低了温度
(3)氮的化合物种类较多,如NH3、NO、NO2、HNO3、硝酸盐等.
①亚硝酸是一种弱酸,能证明亚硝酸是弱电解质的是AD
A.常温下,亚硝酸钠溶液的pH>7
B.亚硝酸能和NaOH发生中和反应
C.用亚硝 酸 溶液做导电性实验,灯泡很暗
D.常温下,将pH=3的亚硝酸溶液稀释10倍,pH<4
②根据酸碱质子理论,凡是能给出质子的分子或离子都是酸,凡是能结合质子的分子或离子都是碱.按照这个理论,下列微粒属于两性物质的是acd
a.H2O b.NO2- c.H2NCH2COOH d.H2PO4- e.H2S
③氮同主族磷元素形成的Na2HPO4溶液显碱性,若向溶液中加入足量的CaCl2溶液,溶液则显酸性,其原因是3Ca2++2HPO42-═Ca3(PO4)2↓+2H+(用离子方程式表示).
(4)X、Y、Z、W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种.下表是常温下浓度均为0.01mol•L-1的X、Y、Z、W溶液的pH.
| 0.01mol•L-1溶液 | X | Y | Z | W |
| pH | 12 | 2 | 8.5 | 4.5 |
(5)N2O5是一种新型绿色硝化剂,其制备可以用硼氢化钠燃料电池作电源,采用电解法制备得到N2O5,工作原理如图.则硼氢化钠燃料电池的负极反应式为BH4-+8OH--8e-=BO2-+6H2O.
4.反应①和②分别是从海藻灰和某种矿石中提取碘的主要反应
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2.
下列说法正确的是( )
①2NaI+MnO2+3H2SO4=2NaHSO4+MnSO4+2H2O+I2
②2NaIO3+5NaHSO3=2Na2SO4+3NaHSO4+H2O+I2.
下列说法正确的是( )
| A. | 两个反应中均为硫元素被氧化 | |
| B. | 反应①、②中生成等量的I2时转移电子数比为1:5 | |
| C. | 氧化性:MnO2>SO42->IO3->I2 | |
| D. | 碘元素在反应①中被还原,在反应②中被氧化 |
6.下列各组离子在指定溶液中能大量共存的是( )
| A. | 室温下,pH=1的溶液中:Na+、NH4+、NO3-、CO32- | |
| B. | 使酚酞呈红色的溶液中:Na+、K+、SiO32-、AlO2- | |
| C. | 含有大量SO32-的溶液中:K+、Ca2+、ClO-、NO3- | |
| D. | 加入Al能放出H2的溶液中:Mg2+、NH4+、HCO3-、Cl- |
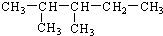 系统命名的名称为2,3-二甲基戊烷.
系统命名的名称为2,3-二甲基戊烷. .
. .
.