题目内容
在t ℃时,将a g NH3完全溶于水,得到V mL溶液,假设该溶液的密度为ρ g·mL-1,质量分数为w,其中含有NH4+的物质的量是b mol,下列叙述正确的是( )
A.溶质的质量分数w=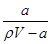 ×100% ×100% |
B.溶质的物质的量浓度c= mol·L-1 mol·L-1 |
C.溶液中c(OH-)=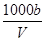 mol·L-1+c(H+) mol·L-1+c(H+) |
| D.向上述溶液中加入V mL水,所得溶液的质量分数大于0.5w |
C
解析试题分析:A、氨水溶液溶质为氨气,该溶液的密度为ρg·mL-1,体积为VmL,所以溶液质量为ρVg,溶质氨气的质量为ag,溶质的质量分数为 ×100%,故A错误;B、a g NH3的物质的量为
×100%,故A错误;B、a g NH3的物质的量为 =
=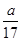 mol,溶液体积为VmL,所以溶液的物质的量浓度为
mol,溶液体积为VmL,所以溶液的物质的量浓度为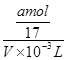 =
= mol·L-1,故B不正确;C、V mL饱和溶液中n(OH-)=n(H+)+n(NH4+)=[c(H+)×10-3+b]mol,所以
mol·L-1,故B不正确;C、V mL饱和溶液中n(OH-)=n(H+)+n(NH4+)=[c(H+)×10-3+b]mol,所以 ,C正确;D、混合前后溶质的质量不变为ag,水的密度比氨水的密度大,即ρg·cm-3<ρ水,等体积Vml混合,混合后溶液的质量大于2ρvg,所以混合后质量分数小于0.5ω,故D不正确.选C。
,C正确;D、混合前后溶质的质量不变为ag,水的密度比氨水的密度大,即ρg·cm-3<ρ水,等体积Vml混合,混合后溶液的质量大于2ρvg,所以混合后质量分数小于0.5ω,故D不正确.选C。
考点:物质的量浓度的相关计算;溶液中溶质的质量分数及相关计算

 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案 新思维寒假作业系列答案
新思维寒假作业系列答案某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解19.2 g(已知硝酸只被还原为NO气体)。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示。下列分析或结果不正确的是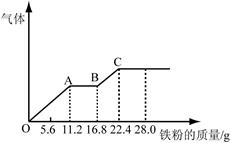
| A.混合酸中HNO3物质的量浓度为2 mol·L-1 |
| B.原混合酸中H2SO4物质的量为0.4 mol |
| C.OA段产生的是NO,AB段的反应为Fe+2Fe3+=3Fe2+,BC段产生氢气 |
| D.第二份溶液中最终溶质为FeSO4 |
向mg镁和铝的混合物中加入适量的稀硫酸,恰好完全反应生成标准状况下的气体bL。向反应后的溶液中加入cmol/L氢氧化钾溶液VmL,使金属离子刚好沉淀完全,得到的沉淀质量为ng。再将得到的沉淀灼烧至质量不再改变为止,得到固体pg。则下列关系不正确的是
| A.c=1000b/11.2V | B.p=m+Vc/125 | C.n=m+17Vc | D.5/3m<p<17/9m |
下列有关化学用语表示正确的是
A.甲醛的电子式: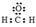 |
B.对甲基苯酚的结构简式: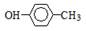 |
C.3,3-二甲基-1-戊烯的键线式: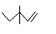 |
D.乙醇分子的比例模型: |
NA为阿伏加德罗常数的数值,下列说法中正确的是
| A.在密闭容器中加入1.5molH2和0.5molN2,充分反应后可得NH3分子数目为NA |
| B.1.0L 0.1mol?L—1Na2CO3溶液中含有的CO32—离子数目为0.1NA |
| C.一定条件下,2.3gNa完全与O2反应生成3.6g产物时失去电子数目为0.1NA |
| D.在标准状况下,2.24L的CH3CH2OH含有NA个分子 |
下列化学用语或模型表示正确的是
A.硝基苯的结构简式: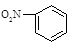 | B.CO2分子比例模型: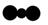 |
C.NH4Cl的电子式: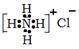 | D.NaCl的晶体模型: |
设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,224mL水含有的电子数为0.1NA |
| B.1L 0.1mol/L硅酸钠溶液中含有0.1NA个SiO32- |
| C.足量的铁粉与lmolCl2在加热条件下充分反应,转移的电子数为3NA |
| D.标准状况下,11.2LCO2和SO2混合气体中含NA个氧原子 |
单质碳和氧化铜在一定温度下反应时,氧化铜可被还原为Cu2O、Cu。现将2.00g C与16.0g CuO的混合物,隔绝空气加热一段时间后,将生成的气体通过足量的澄淸石灰水,共收集到1.12 L气体(标准状况),生成沉淀的质量为5.00 g。下列说法错误的是
| A.反应后的固体混合物中还含有碳 |
| B.反应后的固体混合物中Cu的质量为12.8 g |
| C.反应后的固体混合物总质貴为14.4 g |
| D.反应后的固体混合物中氧化物的物质的量为0.05mol |
FeS2在空气中充分燃烧的化学方程式为4FeS2 + 11O2 2Fe2O3 + 8SO2,若agFeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为
2Fe2O3 + 8SO2,若agFeS2在空气中充分燃烧,并转移N个电子,则阿伏加德罗常数(NA)可表示为
| A.120N/a | B.120a/11N | C.11a/120N | D.120N/11a |