题目内容
17.对于可逆反应4NH3(g)+5O2(g)?4NO(g)+6H2O(g),下列叙述正确的是( )| A. | 达到化学平衡时,4υ正(O2)=5υ逆(NO ) | |
| B. | 若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态 | |
| C. | 恒温、恒容时,当混合气体的密度不再变化时,表示反应达到了化学平衡状态 | |
| D. | 化学反应速率关系是:2υ正(NH3)=3υ正(H2O) |
分析 A、达到化学平衡时,化学反应速率是相等的,且反应速率之比等于方程式的系数之比;
B、达到化学平衡时,化学反应的正逆反应速率是相等的;
C、体积不变密度始终不变;
D、根据化学反应遵循质量守恒以及体积恒定来确定密度的变化情况即可.
解答 解:A、4v正(O2)=5v逆(NO)能证明化学反应的正逆反应速率是相等的,达到了化学平衡状态,故A正确;
B、单位时间内生成x mol NO,同时消耗x mol NH3,则不能说明化学反应的正逆反应速率是相等的,只表示了正反应方向,故B错误;
C、体积不变密度始终不变,所以不能作平衡状态的标志,故C错误;
D、都反映的正反应方向,未体现正与逆的关系,故D错误.
故选A.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案
相关题目
7. 的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )
的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )
 的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )
的同分异构体中,含有苯环且苯环上一氯取代物只有一种的结构共有(不考虑立体异构)( )| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
8.下列物质中含有共价键的离子化合物是( )
| A. | KOH | B. | MgCl2 | C. | CO2 | D. | CH4 |
5.1993年由中国学者和美国科学家共同合成了世界上最大的碳氢分子,其一个分子由1334 个碳原子和1148个氢原子构成.关于此物质,下列说法肯定错误的是( )
| A. | 属烃类化合物 | B. | 常温下是固态 | ||
| C. | 可发生氧化、加成反应 | D. | 可能含381个碳碳叁键 |
12.下列基本操作正确的是( )
| A. | 将固体氢氧化钠用托盘天平直接称量 | |
| B. | 酒精灯的火焰必须用灯帽盖灭,不可用嘴吹灭 | |
| C. | 试管须用试管夹取用,且不能直接加热 | |
| D. | 用燃着的酒精灯去点燃另一个酒精灯 |
9.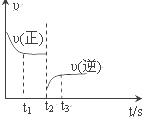 合成氨反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 △H=-92.4kJ•mol.
合成氨反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 △H=-92.4kJ•mol.
如图是该反应速率-时间图象,一定条件下,t1时建立平衡,t2时改变某一条件,t2时改变的条件可能是( )
 合成氨反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 △H=-92.4kJ•mol.
合成氨反应:N2+3H2$?_{催化剂}^{高温、高压}$2NH3 △H=-92.4kJ•mol.如图是该反应速率-时间图象,一定条件下,t1时建立平衡,t2时改变某一条件,t2时改变的条件可能是( )
| A. | 升高温度 | B. | 分离出部分氨气 | C. | 降低压强 | D. | 增大反应物浓度 |
6.用惰性电极电解KCl和CuSO4混合液250mL,经过一段时间后,两极均得到16.8L气体(标准状况),则下列有关描述中,正确的是( )
| A. | 阳极发生的反应只有:2Cl--2e-═Cl2↑ | |
| B. | 两极得到的气体均为混合气体 | |
| C. | 若Cu2+起始浓度为l mol•L-l,则C1-起始浓度为2 mol•L-1 | |
| D. | Cu2+的起始物质的量应小于0.75 mol |
7.室温下,等体积0.5mol/L的①KCl ②FeCl3 ③HF ④Na2CO3四种物质的水溶液中,所含阳离子数目由多到少的顺序是( )
| A. | ④①②③ | B. | ③①②④ | C. | ①④③② | D. | ④②①③ |