题目内容
10.向FeCl3溶液中加入氢氧化钠溶液,化学方程式为:FeCl3+3NaOH═Fe(OH)3↓+3NaCl.分析 氯化铁与氢氧化钠发生复分解反应生成氢氧化铁沉淀和氯化钠,据此写出反应方程式.
解答 解:氯化铁与氢氧化钠发生复分解反应生成氢氧化铁沉淀和氯化钠,化学方程式:FeCl3+3NaOH═Fe(OH)3↓+3NaCl,
故答案为:FeCl3+3NaOH═Fe(OH)3↓+3NaCl.
点评 本题考查了化学方程式的书写,明确反应实质是解题关键,题目不难.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
1.4g NaOH溶解在水中,配成100mL溶液,配好后从中取出10mL溶液,加水稀释至100mL,则稀释后所得溶液物质的量浓度是( )
| A. | 1mol/L | B. | 10mol/L | C. | 0.01mol/L | D. | 0.1mol/L |
18.W,X,Y,Z是短周期元素,其部分性质如表,下列说法正确的是( )
| W | 单质是淡黄色固体 |
| X | 在地壳中的含量居第二位 |
| Y | 原子最外层电子数是电子总数的$\frac{2}{3}$ |
| Z | 第三周期原子半径最小的金属 |
| A. | 气态氢化物的热稳定性:X>W | |
| B. | 最高价氧化物对应水化物的酸性:Y>X | |
| C. | 离子半径:Z>W | |
| D. | X在自然界中以游离态和化合态形式存在 |
5.设NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4LSO3含有NA个分子 | |
| B. | 标准状况下,22.4LCO2与CO的混合气体含NA个分子 | |
| C. | lmolNa2O2与足量CO2反应转移的电子数为2NA | |
| D. | 常温下NA个H2分子的质量约为2g,它所占的体积约为22.4L |
15.实验室需要用480mL 0.1mol•L-1的硫酸铜溶液,以下配制方法正确的是( )
| A. | 称取12.5g胆矾(CuSO4•5H2O),配成500mL溶液 | |
| B. | 称取12.5g胆矾(CuSO4•5H2O),加入500mL水配成溶液 | |
| C. | 称取7.68g无水硫酸铜粉末,加入480mL水配成溶液 | |
| D. | 称取8.0g无水硫酸铜粉末,加入500mL水配成溶液 |
2.在下列各组物质中,属于同系物的是( )
| A. | 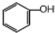 和 和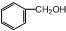 | B. | 丙烷和2,2一二甲基丙烷 | ||
| C. | 乙二醇和丙三醇 | D. | 1,1一二氯乙烷和1,2一二氯乙烷 |
19.下列关于乙烯和苯的性质的叙述中,错误的是( )
| A. | 乙烯能使溴水褪色 | |
| B. | 乙烯能使酸性高锰酸钾溶液褪色 | |
| C. | 将苯加入溴水中,因苯能与溴水发生加成反应而使溴水褪色 | |
| D. | 50~60℃时,在浓硫酸存在下,苯能与浓硝酸反应生成硝基苯 |
20.下列各组离子在无色碱性溶液中可以大量共存的是( )
| A. | Mg2+、NO3-、NH4+ | B. | Na+、K+、CO32- | C. | Fe3+、S042-、Cl- | D. | CH3COO-、Na+、H+ |
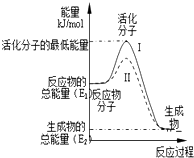 (1)已知:
(1)已知: