题目内容
【题目】铜的相关化合物在生产生活中具有重要的作用。回答下列问题:
(1)铜元素在周期表中的位置是______________,基态铜原子中,核外电子占据最高能层的符号是_________________,占据该最高能层的电子数为__________________。
(2)在一定条件下,金属相互化合形成的化合物称为金属互化物,如Cu9Al4、Cu5Zn8等。某金属互化物具有自范性,原子在三维空间里呈周期性有序排列,该金属互化物属于__________(填“晶体”或“非晶体”)。
(3)铜能与类卤素[(SCN)2]反应生成Cu(SCN)2,1mol(SCN)2分子中含有σ键的数目为______________。 (SCN)2对应的酸有硫氰酸(H-S-C![]() N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________。
N)、异硫氰酸(H-N=C=S)两种。理论上前者沸点低于后者,其原因是____________________________。
(4)铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为________。
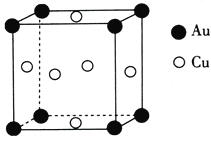
(5)铜与金形成的金属互化物的晶胞结构如图所示,其晶胞边长为a nm,该金属互化物的密度为____________(用含a、NA的代数式表示)g·cm-3。
【答案】 第四周期IB族 N 1 晶体 5NA(或5×6.02×1023) 异硫氰酸分子间可形成氢键,而硫氰酸不能 12 ![]() )
)
【解析】(1)铜原子核电荷数为29,核电电子排布为1s22s22p63s23p64s13d10,在周期表中的位置是第四周期IB族; 基态铜原子中,核外电子占据最高能层的是N层;占据该最高能层的电子数为1;正确答案:第四周期IB族; N ;1。
(2)晶体中原子呈周期性有序排列,有自范性,而非晶体中原子排列相对无序,无自范性,题述金属互化物属于晶体;正确答案:晶体。
(3)类卤素(SCN)2的结构式为N≡C—S—S—C≡N,1mol(SCN)2中含σ键的数目为5NA。异硫氰酸(H—N===C===S)分子中N原子上连接有H原子,分子间能形成氢键,故沸点高;正确答案;5NA(或5×6.02×1023) ;异硫氰酸分子间可形成氢键,而硫氰酸不能。
(4)在金属晶体的最密堆积中,对于每个原子来说,在其周围的原子有与之同一层上有六个原子和上一层的三个及下一层的三个,故每个原子周围都有12个原子与之相连;铜晶体中铜原子的堆积方式为面心立方堆积,每个铜原子周围距离最近的铜原子个数为12;正确答案:12。
(5)根据均摊法,铜与金形成的金属互化物晶胞中Cu的个数为6×![]() =3,Au的个数为8×
=3,Au的个数为8×![]() =1,该金属互化物的化学式为Cu3Au,该金属互化物的密度为
=1,该金属互化物的化学式为Cu3Au,该金属互化物的密度为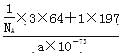 g·cm-3=
g·cm-3=![]() g·cm-3;正确答案:
g·cm-3;正确答案:![]() 。
。

 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案