题目内容
2.100mL 6mol•L-1 H2SO4跟过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量( )| A. | 碳酸钠(固体) | B. | 水 | C. | 硫酸钾溶液 | D. | 浓硝酸 |
分析 为了减缓反应进行的速率,可降低浓度、温度,但又不影响生成氢气的总量,则氢离子的总物质的量不变,以此解答该题.
解答 解:A.加入碳酸钠,消耗硫酸,浓度降低,反应速率减小,且生成氢气的总量减小,故A错误;
B.加入水,氢离子浓度降低,则反应速率减小,但生成氢气的总量不变,故B正确;
C.加入硫酸钾溶液,氢离子浓度降低,则反应速率减小,但生成氢气的总量不变,故C正确;
D.加入浓硝酸,生成NO气体,影响生成氢气的总量,故D错误.
故选BC.
点评 本题考查化学反应速率的影响因素,侧重于基础知识的考查,注意把握影响化学反应速率的因素,把握题目要求,为解答该题的关键,难度不大.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
13.某有机物的结构简式为 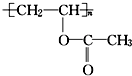 ,下列关于该有机物叙述不正确的是( )
,下列关于该有机物叙述不正确的是( )
 ,下列关于该有机物叙述不正确的是( )
,下列关于该有机物叙述不正确的是( )| A. | 1 mol 该有机物与 NaOH 溶液完全反应时,消耗 NaOH 1 mol | |
| B. | 该有机物水解所得产物能发生取代反应 | |
| C. | 该有机物可通过加聚反应生成 | |
| D. | 该有机物分子中含有双键 |
10.若从溴水中把溴萃取出来,可选用的萃取剂是( )
| A. | 水 | B. | 无水酒精 | C. | 四氯化碳 | D. | 氢氧化钠溶液 |
17.下列各组离子能大量共存的是( )?
| A. | K+、NH4+、SO42-、NO3- | B. | OH-、K+、NH4+、Cl- | ||
| C. | Fe3+、Cl-、Na+、OH- | D. | Fe2+、H+、SO32-、NO3- |
7.某溶液与Al反应能放出H2,下列离子在该溶液中一定能大量共存的是( )
| A. | K+、Ca2+、HCO3-、Cl- | B. | Na+、K+、Cl-、SO42- | ||
| C. | NH4+、K+、Cl-、SO32- | D. | K+、Cl-、NO3-、SO42- |
14.对于以下反应:A(s)+3B(g)?2C(g)+D(g),在一定温度和容积固定的容器中,下列判断正确的是( )
| A. | 若反应是放热反应,升高温度,正反应速率增大 | |
| B. | 往容器中通入稀有气体He,由于压强增大,所以反应速率增大 | |
| C. | 往容器中加入少量A,反应速率增大 | |
| D. | 当容器内的压强不再变化,可以判断反应已经达到平衡 |
11.有核磁共振氢谱如图,下列有机物符合该图谱的是( )
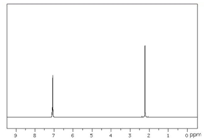

| A. |  | B. | 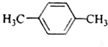 | C. | 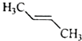 | D. | 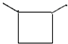 |
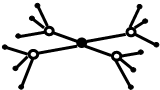 周期表前四周期的元素X、Y、Z、T、W,原子序数依次增大.X的核外电子总数与其周期数相同,Y基态原子的p电子数比s电子数少1个,Z基态原子的价电子层中有2个未成对电子,T与Z同主族,W基态原子的M层全充满,N层只有一个电子.回答下列问题:
周期表前四周期的元素X、Y、Z、T、W,原子序数依次增大.X的核外电子总数与其周期数相同,Y基态原子的p电子数比s电子数少1个,Z基态原子的价电子层中有2个未成对电子,T与Z同主族,W基态原子的M层全充满,N层只有一个电子.回答下列问题: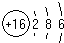 ,W基态原子的电子排布式为[Ar]3d104s1.
,W基态原子的电子排布式为[Ar]3d104s1.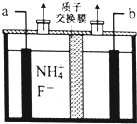 (1)某催化剂可将汽车尾气中的CO、NO转化为无毒气体.已知:
(1)某催化剂可将汽车尾气中的CO、NO转化为无毒气体.已知: