题目内容
Fe原子或离子外围有较多能量相近的空轨道能与一些分子或离子形成配合物.
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是 .
②六氰合亚铁离子[Fe(CN)6]4-中不存在 .
A.共价键 B.非极性键 C.配位键 D.σ键 E.π键
③写出一种与CN-互为等电子体的单质分子式 .
①与Fe原子或离子形成配合物的分子或离子应具备的结构特征是
②六氰合亚铁离子[Fe(CN)6]4-中不存在
A.共价键 B.非极性键 C.配位键 D.σ键 E.π键
③写出一种与CN-互为等电子体的单质分子式
考点:配合物的成键情况,“等电子原理”的应用
专题:化学键与晶体结构
分析:①形成配离子具备的条件为:中心原子具有空轨道,配体具有孤对电子对;
②六氰合亚铁离子[Fe(CN)6]4-中Fe2+与CN-形成配位键,CN-中存在C≡N三键,为极性共价键,三键中有1个σ键2个π键;
③CN-中C原子与1个单位负电荷用N原子替换可得CN-等电子体的单质;
②六氰合亚铁离子[Fe(CN)6]4-中Fe2+与CN-形成配位键,CN-中存在C≡N三键,为极性共价键,三键中有1个σ键2个π键;
③CN-中C原子与1个单位负电荷用N原子替换可得CN-等电子体的单质;
解答:
解:①形成配离子具备的条件为:中心原子具有空轨道,配体具有孤对电子对,故答案为:具有孤对电子;
②六氰合亚铁离子[Fe(CN)6]4-中Fe2+与CN-形成配位键,CN-中存在C≡N三键,为极性共价键,三键中有1个σ键2个π键,所以CN-中共价键、配位键、σ键、π键,故答案为:B;
③CN-中C原子与1个单位负电荷用N原子替换可得CN-等电子体的单质为N2,故答案为:N2;
②六氰合亚铁离子[Fe(CN)6]4-中Fe2+与CN-形成配位键,CN-中存在C≡N三键,为极性共价键,三键中有1个σ键2个π键,所以CN-中共价键、配位键、σ键、π键,故答案为:B;
③CN-中C原子与1个单位负电荷用N原子替换可得CN-等电子体的单质为N2,故答案为:N2;
点评:本题主要考查了配合物的形成条件及其中的化学键类型、等电子体,难度不大,注重对基础知识的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
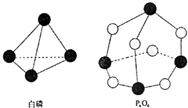 化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ?mol-1)P-P:198 P-O:360 O═O:498则反应P4(白磷)+3O2→P4O6的能量变化为( )
化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol化学键时释放(或吸收)出的能量.已知白磷和P4O6的分子结构如右图所示,现提供以下化学键的键能(kJ?mol-1)P-P:198 P-O:360 O═O:498则反应P4(白磷)+3O2→P4O6的能量变化为( )| A、释放1638kJ的能量 |
| B、吸收1638kJ的能量 |
| C、释放126kJ的能量 |
| D、吸收126kJ的能量 |
同周期的X、Y、Z三种元素,已知最高价氧化物的水化物酸性由强到弱顺序为HXO4>H2YO4>H3ZO4,则下列判断错误的是( )
| A、原子序数:X>Y>Z |
| B、非金属性:X>Y>Z |
| C、原子半径:X>Y>Z |
| D、气态氢化物的稳定性:HX>H2Y>ZH3 |