题目内容
【题目】污水治理越来越引起人们重视,可以通过膜电池除去废水中的乙酸钠和对氯苯酚![]() ,其原理如图所示,下列说法不正确的是
,其原理如图所示,下列说法不正确的是
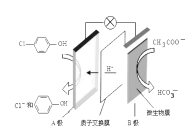
A.电流方向从B极沿导线经小灯泡流向A极
B.A为电池的正极,发生还原反应
C.A极的电极反应式为:![]()
D.当外电路中有0.2mole-转移时,进入A极区的H+的个数为0.2NA
【答案】A
【解析】
原电池中阳离子移向正极,根据原电池中氢离子的移动方向可知A为正极,正极有氢离子参与反应,电极反应式为Cl-![]() -OH+2e-+H+═
-OH+2e-+H+═![]() -OH+Cl-,电流从正极经导线流向负极,以此解答该题。
-OH+Cl-,电流从正极经导线流向负极,以此解答该题。
原电池中阳离子移向正极,根据原电池中氢离子的移动方向可知A为正极,正极有氢离子参与反应,电极反应式为Cl![]() OH+2e+H+═
OH+2e+H+═![]() OH+Cl,电流从正极经导线流向负极。
OH+Cl,电流从正极经导线流向负极。
A. 电流从正极A沿导线流向负极B,故A错误;
B.根据分析,A为正极,发生还原反应,故B正确;
C.A为正极,正极有氢离子参与反应,电极反应式为Cl![]() OH+2e+H+═
OH+2e+H+═![]() OH+Cl,故C正确;
OH+Cl,故C正确;
D. 据电荷守恒,当外电路中有0.2mole转移时,通过质子交换膜的H+的个数为0.2NA,故D正确;
答案选A。

练习册系列答案
相关题目
【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验 | 现象 | 结论 |
A | 向酸性高锰酸钾溶液中通入SO2 | 溶液颜色褪去 | SO2具有漂白性 |
B | 将少量铜粉加入FeCl3溶液中 | 铜粉消失 | 还原性:Cu>Fe2+ |
C | 向溶液X中先滴加稀硝酸,再滴加氯化钡溶液 | 有白色沉淀生成 | 溶液X中含有SO |
D | 锌与稀硫酸反应制取氢气时,加入少量硫酸铜溶液 | 反应速率加快 | Cu2+起催化作用 |
A.AB.BC.CD.D