题目内容
9.写出下列反应的离子方程式.(1)碳酸钙与稀盐酸
(2)氢氧化钡溶液与硫酸铜溶液
(3)碳酸氢钙溶液与氢氧化钙.
分析 (1)反应生成氯化钙和水、二氧化碳;
(2)反应生成硫酸钡和氢氧化铜沉淀;
(3)反应生成碳酸钙和水.
解答 解:(1)碳酸钙与稀盐酸,离子方程式:CaCO3+2H+=Ca2++CO2↑+H2O;
故答案为:CaCO3+2H+=Ca2++CO2↑+H2O;
(2)氢氧化钡溶液与硫酸铜溶液,离子方程式:Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓;
故答案为:Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓;
(3)碳酸氢钙溶液与氢氧化钙,离子方程式:Ca2++OH-+HCO3-=CaCO3↓+H2O;
故答案为:Ca2++OH-+HCO3-=CaCO3↓+H2O.
点评 本题考查了离子方程式书写,明确反应实质及离子方程式书写是解题关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
20.下列叙述正确的是( )
| A. | 1mol任何气体的体积都约为22.4L | |
| B. | 标准状况下,氧气的体积约为22.4L | |
| C. | 在同温同压下,22g CO2与11.2L HCl含有相同的分子数 | |
| D. | 标准状况下,32g氧气的体积约是22.4L |
4.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法正确的是( )
| A. | 元素X与Z、Y 与W形成的化合物都为离子化合物 | |
| B. | 元素X与Y,Z与Y形成的二元化合物都只有一种 | |
| C. | Y、Z、W三种元素形成的离子半径随原子序数的增加而增大 | |
| D. | 元素W、R的最高价氧化物的水化物都是强酸 |
1.绿原酸的结构简式如图,下列有关绿原酸的说法错误的是( )
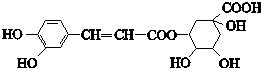
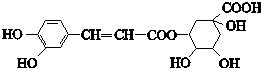
| A. | 分子式为C16H18O9 | |
| B. | 能与NaHCO3反应 | |
| C. | 能发生取代反应、氧化反应和消去反应 | |
| D. | 1 mol绿原酸最多与6 mol Br2反应 |
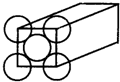 金晶体是面心立方体,立方体的每个面5个金原子紧密堆砌(如图其余各面省略),金原子半径为1.44×10-10 m,Au的摩尔质量为197g/mol.求:
金晶体是面心立方体,立方体的每个面5个金原子紧密堆砌(如图其余各面省略),金原子半径为1.44×10-10 m,Au的摩尔质量为197g/mol.求: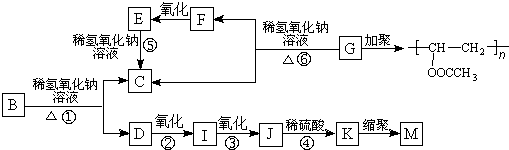
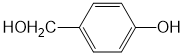 ,F:CH3CHO.
,F:CH3CHO. ,
,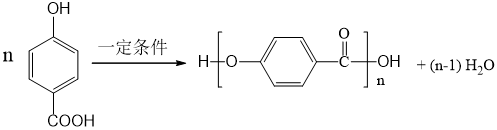 .
.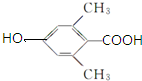 ,
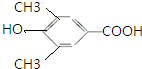
,
 的同分异构体:
的同分异构体: 、
、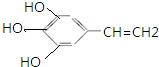 .
.