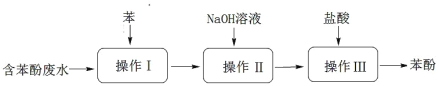
题目内容
【题目】右图装置中发生反应的离子方程式为:Zn+2H+=Zn2++H2↑,下列说法错误的是
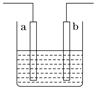
A. a、b不可能是同种材料的电极
B. 该装置可能是电解池,电解质溶液为稀盐酸
C. 该装置可能是原电池,电解质溶液为稀盐酸
D. 该装置可看作是铜-锌原电池,电解质溶液是稀硫酸
【答案】A
【解析】试题分析:A、如果此装置是电解池装置,阴阳两极为锌,电解质溶液是硫酸溶液,故说法错误;B、如果是电解质,阳极反应式:Zn-2e-=Zn2+,阴极:2H++2e-=H2↑,故说法正确;B、如果是原电池,负极为Zn,反应式为Zn-2e-=Zn2+,正极反应式:2H++2e-=H2↑,故说法正确;D、锌比铜活泼,锌作负极,负极为Zn,反应式为Zn-2e-=Zn2+,正极反应式:2H++2e-=H2↑,故说法正确;铜作正极,

练习册系列答案
相关题目
【题目】中学化学中很多“规律”都有适用范围,下列根据有关“规律”推出的结论正确的是( )
选项 | 规律 | 结论 |
A | 元素的非金属性较强,其单质也越活泼 | 磷单质比 |
B | 反应物浓度越大,反应速率越快 | 常温下,相同的铝片中分别加入足量的浓硝酸、稀硝酸,浓硝酸中铝片先溶解完全 |
C | 结构和组成相似的物质,沸点随相对分子质量增大而升高 |
|
D | 溶解度小的沉淀易向溶解度更小的沉淀转化 | ZnS沉淀中滴加 |
A.AB.BC.CD.D