��Ŀ����
14��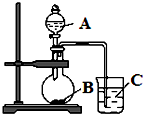 ij�о���ѧϰС�������һ��ʵ�飬��֤Ԫ�������ɣ�
ij�о���ѧϰС�������һ��ʵ�飬��֤Ԫ�������ɣ���1����ͬѧ��a��b��c��d��ֻ�ձ���ֱ����50mL��ˮ���ٷֱ�μӼ��η�̪��Һ�����μ����С������ƣ�Na����þ��Mg��������Al�����أ�K�������飬�۲�����
�ټ�ͬѧ���ʵ���Ŀ������֤��ͬһ���壬���ϵ���Ԫ�ص�Ԫ��ʧ������������ǿ��ͬһ���ڣ������ң�Ԫ��ʧ��������������
�ڷ�Ӧ����ҵ��ձ��������D������ĸ��A���� B��þ C���� D���أ�
��д��a�ձ������Ӧ�����ӷ���ʽ2Na+2H2O=2Na++2OH-+H2����
��ʵ���з���b��c��ֻ�ձ��м���û��ʲô����Ҫ��ﵽʵ���Ŀ�ģ��������ѡ�����к��ʵķ���BC
A����þ�����Ľ����黻�ɽ�����ĩ B�����ձ��е���ˮ������ˮ
C�����ձ��е���ˮ�������� D�����ձ��е���ˮ��������������Һ
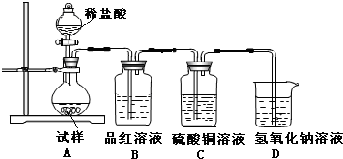
��2����ͬѧ���ʵ����֤���ǽ���Ԫ�صķǽ�����Խǿ������ۺ���������Ծ�Խǿ�����������ͼװ������֤̼��������Ԫ�صķǽ�����ǿ������ͬѧ��Ƶ�ʵ���ֱ��֤�������������ǿ������֪A��ǿ�ᣬ��Ũ��Һ�ڳ����¿���ͭ��Ӧ��B�ǿ�״���壻�ձ���ʢ��C��ˮ��Һ����Һ©���Ļ�����C�пɹ۲쵽��ɫ��״�������ɣ�
��д����ѡ�����ʵĻ�ѧʽ��A��HNO3�� C��Na2SiO3����K2SiO3����
��д����ƿ�з�����Ӧ�Ļ�ѧ����ʽ��2HNO3+CaCO3=Ca��NO3��2+H2O+CO2����
��̼������������Ԫ�صĵõ���������ǿ����˳��Ϊ����̼���裮
���� ��1���ٸ���Ԫ�������ɿ�֪��ͬһ���ڣ������ң�ʧ��������������Ԫ�ؽ�����������
�����жϽ�����ǿ����Ȼ����ݽ�����Խǿ��������ˮ��ӦԽ���ң�
������ˮ��Ӧ�����������ƺ��������������ӷ���ʽ����д������д��
�ܷ�Ӧ�������ԣ�˵����Ӧ����С������Ӱ�����ʵ����ط�����
��2������ǿ���Ʊ�������У�A��ǿ�ᣬ�����¿���ͭ��Ӧ��Ϊ���B�ǿ�״���壬��Һ©���Ļ�����C�пɹ۲쵽��ɫ�������ɣ���BΪ̼��ơ�CΪ�����ƣ��Դ˽��
��� �⣺��1����ͬһ���ڣ������ң�ԭ��ʧ����������������Ԫ�ؽ�����������
�ʴ�Ϊ��������
�ڽ����ԣ�K��Na��Mg��Al��������Խǿ��������ˮ��ӦԽ���ң��ʷ�Ӧ����ҵ��ձ���D��
�ʴ�Ϊ��D��
������ˮ��Ӧ�����������ƺ���������Ӧ�����ӷ���ʽ��2Na+2H2O=2Na++2OH-+H2����
�ʴ�Ϊ��2Na+2H2O=2Na++2OH-+H2����
�ܷ�Ӧ�������ԣ�˵����Ӧ����С�������¶ȿ��Լӿ����ʣ�������ˮ��Ϊ��ˮ����ˮ��Ϊ������������Һ�������ӵ�Ũ�ȣ����Լӿ����ʣ�
�ʴ�Ϊ��BC��
��2��������ǿ���Ʊ�������У�A��ǿ�ᣬ�����¿���ͭ��Ӧ�����B�ǿ�״���壬��Һ©���Ļ�����C�пɹ۲쵽��ɫ�������ɣ���BΪ̼��ơ�CΪ�����ƻ����أ�
�ʴ�Ϊ��HNO3��Na2SiO3����K2SiO3����
����ƿ�з���������̼��Ƶķ�Ӧ������ʽΪ2HNO3+CaCO3=Ca��NO3��2+H2O+CO2����
�ʴ�Ϊ��2HNO3+CaCO3=Ca��NO3��2+H2O+CO2����
��Ԫ�صķǽ�����Խǿ����Ӧ������������ˮ���������Խǿ����ʵ���֪���ԣ��������̼�ᣬ̼����ڹ��ᣬ��ǽ����Ե���̼���裬
�ʴ�Ϊ������̼���裮
���� ���⿼������������ʵ�鷽������ƣ�������ѧ���ķ���������ʵ�������Ŀ��飬���⽫Ԫ�ؼ��仯���Ԫ����������ʵ��֪ʶ������������н�ǿ���ۺ��ԣ��ѶȲ���

 �ǻ�С��ϰϵ�д�
�ǻ�С��ϰϵ�д���O2 N2 Cu Si ��HCl HBr H2S HNO3��CaO Na2O CuO Al2O3
��NH4Cl NaOH NaAlO2 K2CO3
��1����д�±��հף�
| �� | ���� | ���� | ���� | ���� |
| ����� | �ǽ��� | ������ | ���������� | |
| �������� | NaOH |
A ��״���෨ B ������෨
��3�������Т٢������ʷ�Ӧ����0.6molNO����ת�Ƶĵ�����ĿΪ0.18NA�����������õ�HNO3���ʵ���Ϊ1.8mol��
��4��д�����Тۢ������ʷ�Ӧ�����ӷ���ʽ��Al2O3+2OH-=2AlO2-+H2O��
 ʵ��������һδ֪Ũ�ȵ�ϡ���ᣬijѧ��Ϊ�ⶨ�����Ũ����ʵ�����н�������ʵ�飺�����������գ�
ʵ��������һδ֪Ũ�ȵ�ϡ���ᣬijѧ��Ϊ�ⶨ�����Ũ����ʵ�����н�������ʵ�飺�����������գ���1������100mL 0.10mol/L NaOH����Һ��
��2��ȡ20.00mL����ϡ������Һ������ƿ�У����μ�2��3�η�̪��ָʾ�������Լ����Ƶı�NaOH��Һ���еζ����ظ������ζ�����2��3�Σ���¼�������£�
| ʵ���� | NaOH��Һ��Ũ�� ��mol/L�� | �ζ����ʱ��NaOH��Һ����������mL�� | ����������Һ����� ��mL�� |
| 1 | 0.10 | 22.50 | 20.00 |
| 2 | 0.10 | 18.56 | 20.00 |
| 3 | 0.10 | 18.54 | 20.00 |
�ڸ����������ݣ��ɼ�����������Ũ��ԼΪ0.093mol/L��������λ��Ч���֣�
��NaOH��ҺҪʹ�������ĸ������ң���� ���ң���
��������ʵ���У����в���������������ȷ������ɲⶨ���ƫ�ߵ���D��F������ѡ�۷֣���ѡ��һ����2�֣���ѡ��ѡ���÷֣�
A���ζ��յ����ʱ���Ӷ���
B����ʽ�ζ���ʹ��ǰ��ˮϴ��δ�ô���������Һ��ϴ
C����ƿˮϴ��δ����
D������ǰNaOH�����л���Na2CO3����
E�����ƺõ�NaOH����Һ���治��������������е�CO2��Ӧ������Na2CO3
F����ʽ�ζ��ܼ��첿�������ݣ��ζ�����ʧ��
H2��g��+$\frac{1}{2}$O2��g���TH2O��g����H=a kJ•mol-1
H2��g��+$\frac{1}{2}$O2��g���TH2O��l����H=b kJ•mol-1
2H2��g��+O2��g���T2H2O��l����H=c kJ•mol-1
���й������ǵı�����ȷ���ǣ�������
| A�� | ���Ƕ������ȷ�Ӧ | B�� | a��b��c��Ϊ��ֵ | ||
| C�� | ��Ӧ�ȵĹ�ϵ��2b=c | D�� | ��Ӧ�ȵĹ�ϵ��a=b |