题目内容
3.某次发射火箭,用N2H4(肼)在NO2中燃烧,生成N2、液态H2O.已知:①$\frac{1}{2}$N2(g)+O2(g)═NO2(g)△H1=+33.6kJ/mol
②N2H4(g)+O2(g)═N2(g)+2H2O(l)△H2=-534kJ/mol
③N-H键、N≡N键、O=O键、O-H键的键能分别为391kJ•mol-1、946kJ•mol?1、495kJ•mol?1、463kJ•mol?1,N2H4的结构式为:

(1)求N2H4(肼)中N-N的键的键能205kJ•mol-1
(2)请写出该发射火箭反应的热化学方程式:2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-1153.2kJ•mol-1 .
分析 (1)根据焓变等于反应物键能之和-生成物键能之和计算;
(2)①$\frac{1}{2}$N2(g)+O2(g)═NO2(g)△H1=+33.6kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-543kJ•mol-1
依据盖斯定律②×2-①×2计算得到.
解答 解:(1)在反应N2H4(g)+O2(g)═N2(g)+2H2O(l)△H2=-534kJ/mol,设N2H4(肼)中N-N的键的键能为xkJ/mol,则根据焓变等于反应物键能之和-生成物键能之和,所以△H2=-534kJ/mol=391×4+x+495-946-463×4,解得x=205kJ/mol
故答案为:205;
(2)①$\frac{1}{2}$N2(g)+O2(g)═NO2(g)△H1=+33.6kJ/mol
②N2H4(g)+O2(g)=N2(g)+2H2O(g)△H=-543kJ•mol-1
依据盖斯定律②×2-①×2得到,2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-543×2-33.6×2=-1153.2kJ•mol-1;
故答案为:2N2H4(g)+2NO2(g)=3N2(g)+4H2O (g)△H=-1153.2kJ•mol-1 .
点评 本题考查了热化学方程式的计算和盖斯定律的计算应用,理解实质,掌握基础是解题关键,题目较简单.

练习册系列答案
 出彩同步大试卷系列答案
出彩同步大试卷系列答案
相关题目
8.下列化学反应的离子方程式书写正确的是( )
| A. | FeCl3溶液与Cu粉反应:Cu+2Fe3+═Cu2++2Fe2+ | |
| B. | 钠与水反应:Na+2H2O=Na++2OH-+H2↑ | |
| C. | 氯气与水反应:Cl2+H2O?2H++Cl-+ClO- | |
| D. | 氯化铝溶液与过量氨水反应:3NH3•H2O+Al3+=Al(OH)3↓+3NH4+ |
8.下列表示物质结构的化学用语或模型正确的是( )
| A. | CH4分子的比例模型: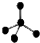 | B. | 氯原子的结构示意图: | ||
| C. | NH3分子的电子式: | D. | CO2分子的结构式:O=C=O |
15.下列各组中的两种物质熔化时克服的作用力不同的是( )
| A. | 干冰、SO3晶体 | B. | 食盐、烧碱 | ||
| C. | 氧化镁、冰 | D. | 固态氮气、固态氧气 |
13.设NA表示阿伏加德罗常数的值,下列叙述不正确的是( )
| A. | 含有NA个氦原子的氦气在标准状况下的体积约为11.2L | |
| B. | 标准状况下,9克H2O 含有的分子数为0.5NA | |
| C. | 常温常压下,32g O2和O3的混合气体所含原子数为2NA | |
| D. | 1mol Fe和足量稀盐酸反应,铁失去的电子数为2NA |
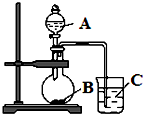 某研究性学习小组设计了一组实验,验证元素周期律.
某研究性学习小组设计了一组实验,验证元素周期律.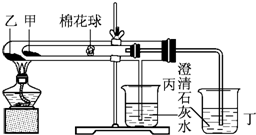 下列是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察下图的实验装置,分析实验原理,回答下列问题:
下列是某兴趣小组根据课本实验设计的一个能说明碳酸钠与碳酸氢钠热稳定性的套管实验.请观察下图的实验装置,分析实验原理,回答下列问题: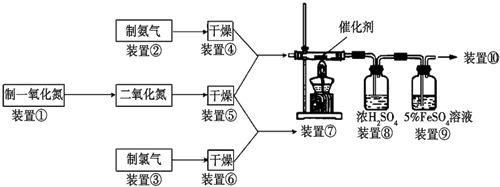
 实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.
实验室需要0.1mol/LNaOH溶液450mL和0.5mol/L的硫酸溶液500mL.根据这两种溶液的配制情况回答下列问题.