题目内容
2.晶体硼由105B和115B两种同位素原子构成.已知5.4g晶体硼全部转化成B2H6(硼烷)气体时,可得标准状况下5.6L硼烷,则下列说法正确的是( )| A. | 晶体中105B和115B两种同位素原子的质量比为1:4 | |
| B. | 5.4 g该晶体硼所含中子为2.9 mol | |
| C. | 等质量的分别由105B和115B构成的晶体硼所含中子数之比为6:5 | |
| D. | 若碳原子质量为w g,则105B原子的质量为10w g |
分析 标准状况下5.6L硼烷的物质的量为$\frac{5.6L}{22.4L/mol}$=0.25mol,则B原子物质的量为0.25mol×2=0.5mol,故硼的相对原子质量为$\frac{5.4}{0.5}$=10.8,设105B和115B的物质的量分别为xmol、ymol,则$\left\{\begin{array}{l}{10x+11y=5.4}\\{\frac{10x+11y}{x+y}=10.8}\end{array}\right.$,解得x=0.1,y=0.4.
A.根据m=nM计算105B和115B的质量之比;
B.根据质量数=质子数+中子数计算105B和115B原子含有的中子数,进而计算中子物质的量;
C.根据n=$\frac{m}{M}$计算105B和115B的物质的量之比,结合原子含有中子数计算;
D.原子质量之比等于相对原子质量之比,近似为原子的质量数之比.
解答 解:标准状况下5.6L硼烷的物质的量为$\frac{5.6L}{22.4L/mol}$=0.25mol,则B原子物质的量为0.25mol×2=0.5mol,故硼的相对原子质量为$\frac{5.4}{0.5}$=10.8,设105B和115B的物质的量分别为xmol、ymol,则$\left\{\begin{array}{l}{10x+11y=5.4}\\{\frac{10x+11y}{x+y}=10.8}\end{array}\right.$,解得x=0.1,y=0.4.
A.105B和115B的质量之比为0.1×10:0.4×11=5:22,故A错误;
B.105B原子中子数为10-5=5,115B原子含有的中子数为11-5=6,故该5.4g硼晶体中含有中子为0.1mol×5+0.4mol×6=2.9mol,故B正确;
C.等质量的分别由105B和115B构成的晶体硼所含中子数之比为$\frac{m}{10}$×5:$\frac{m}{11}$×6=11:12,故C错误;
D.原子的质量之比等于相对原子质量之比,近似为原子的质量数之比,105B原子的质量与碳原子质量之比不是10:1关系,故D错误,
故选B.
点评 本题考查物质的量有关计算、原子结构等,难度中等,注意对基础知识的理解掌握.

 快捷英语周周练系列答案
快捷英语周周练系列答案| A. | C6H5O-+CO2+H2O→C6H5OH+HCO3- | |
| B. | C6H5OH+OH-→C6H5O-+H2O | |
| C. | CH3CHO+2[Ag(NH3)2]++2OH-→CH3COONH4+2Ag↓+3NH3+H2O | |
| D. | CH3CHO+2[Ag(NH3)2]++2OH-→CH3COO-+NH4++2Ag↓+3NH3+H2O |

(1)已知:C(s)+O2(g)=CO2(g)△H=-393kJ•mol-1;
2CO(g)+O2(g)=2CO2(g)△H=-566kJ•mol-1;
2H2(g)+O2(g)=2H2O(g)△H=-484kJ•mol-1
将水蒸气喷到灼热的炭上可实现炭的气化(制得CO、H2),该反应的热化学方程式为C(s)+H2O(g)=CO(g)+H2(g),△H=+132kJ•mol-1.
(2)将一定量CO(g)和H2O(g)分别通入容积为2L的恒容密闭容器中,一定条件下发生反应为CO(g)+H2O(g)?CO2(g)+H2(g),得到如下三组实验数
| 实验编号 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| H2O | CO | CO2 | |||
| 1 | 500 | 4 | 8 | 3.2 | 4 |
| 2 | 750 | 2 | 4 | 0.8 | 3 |
| 3 | 750 | 2 | 4 | 0.8 | 1 |
②实验1中,0~4min时段内,以v(H2)表示的反应速率为0.4mol/(L•min).若在此温度下H2O(g)、CO(g)起始量分别为2mol、4mol,则此反应的平衡常数为$\frac{8}{3}$.
③实验2达到平衡时CO的转化率为20%.
④实验3与实验2相比,改变的条件是加催化剂;
请在如图1坐标中画出“实验2”与“实验3”中c(CO2)随时间变化的曲线,并作标注实验编号.
(3)CO与H2一定条件下反应生成甲醇(CH3OH),甲醇是一种燃料,可利用甲醇设计一个燃料电池,用KOH溶液作电解质溶液,多孔石墨做电极,该电池的负极反应式为CH3OH-6e-+8OH-═CO32-+6H2O.
(4)一定条件下,如图2示装置可实现有机物的电化学储氢(忽略其它有机物),则阴极的电极反应式为
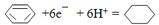 .
. | 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K=1.77×10-4 | K=4.9×10-10 | K1=4.3×10-7,K2=5.6×10-11 |
| A. | 在NaHCO3溶液中:c(OH-)-c(H+)=c(H2CO3)-c(CO32-) | |
| B. | 向NaCN溶液中通入少量CO2的离子方程式:2CN-+H2O+CO2=2HCN+CO32- | |
| C. | 中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者大于后者 | |
| D. | 等物质的量浓度的各溶液pH关系为:pH(NaHCO3)>pH(NaCN)>pH(HCOONa) |
| A. | 标准状况下,33.6 L 氟化氢中含有氟原子的数目为1.5NA | |
| B. | pH均为5的NH4Cl和NaHSO4溶液中水电离出的氢离子数目均为10-5NA | |
| C. | 在1L 0.1 mol•L-1CuSO4溶液中,阴离子总数大于0.1 NA | |
| D. | 某密闭容器盛有0.1molN2和0.3molIH2,在一定条件下充分反应,转移电子的数目为 NA |
 6
6 7
7 6
6 6.
6.