题目内容
10.某化学兴趣小组欲选用下列装置和药品制取纯净乙炔并进行有关乙炔性质的探究,试回答下列问题.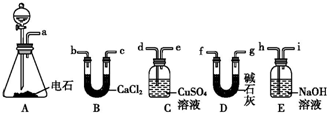
(1)A中制取乙炔的化学方程式为CaC2+2H2O→C2H2↑+Ca(OH)2.
(2)制乙炔时,旋开分液漏斗的活塞,使水缓慢滴下的原因是控制反应速率,使产生的气流稳定,避免产生的泡沫进入导管.
(3)用电石制得的乙炔中常含有H2S、PH3等杂质,除去杂质应选用C(填序号,下同)装置,气体应从d进;干燥乙炔最好选用D装置.
(4)为了探究乙炔与HBr发生加成反应后的有关产物,进行以下实验:
纯净乙炔气$→_{催化剂}^{HBr}$混合液$\stackrel{操作a}{→}$有机混合物Ⅰ$\stackrel{NaOH溶液}{→}$混合液$\stackrel{操作b}{→}$有机混合物Ⅱ
①操作b的名称是蒸馏(或分馏);
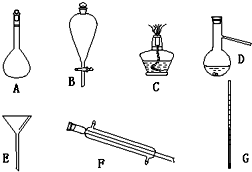
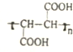
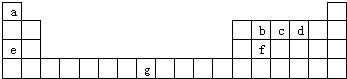
②有机混合物Ⅰ可能含有的物质是CH2═CHBr、CH3-CHBr2、CH2Br-CH2Br (写出其中一种的结构简式).
分析 (1)制取乙炔使用电石(碳化钙)和水反应;
(2)由于CaC2与H2O反应剧烈,产生C2H2的速率很快,故应控制H2O的滴速来达到控制反应速率,防止产生的泡沫进入导气管;
(3)根据乙炔制取实验分析;
(4)分离有机物一般是根据其沸点差异进行分离.有机反应有副产物.
解答 解:(1)制取乙炔使用电石(碳化钙)和水反应生产乙炔和氢氧化钙:CaC2+2H2O→C2H2↑+Ca(OH)2,
故答案为:CaC2+2H2O→C2H2↑+Ca(OH)2;
(2)由于CaC2与H2O反应剧烈,产生C2H2的速率很快,故应控制H2O的滴速来达到控制反应速率,防止产生的泡沫进入导气管,
故答案为:控制反应速率,使产生的气流稳定,避免产生的泡沫进入导管;
(3)H2S、PH3等杂质均能被CuSO4溶液吸收,硫化氢和硫酸铜反应生成CuS沉淀,PH3易溶于水.根据“长进短出”的原则,气体应从C装置中的d导入.碱石灰是NaOH、CaO的混合物,其干燥效率优于CaCl2,故用D装置干燥C2H2,
故答案为:C;d;D;
(4)CH≡CH与HBr发生加成反应时,若CH≡CH中断裂一个键,则与HBr加成可得CH2═CHBr,CH2═CHBr能继续与HBr加成得到CH3-CHBr2、BrCH2-CH2Br.分离有机物一般是根据其沸点差异,采用蒸馏或分馏方法,
故答案为:①蒸馏或分馏;②CH2═CHBr、CH3-CHBr2、CH2Br-CH2Br.
点评 本题考查乙炔的实验室制法及其性质,侧重基础知识的考查,利用所学知识即可完成,题目难度中等.

练习册系列答案
相关题目
20.用下列实验装置进行相应实验,能达到实验目的是( )
| 选项 | A | B | C | D |
| 装置 | 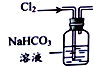 | 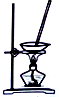 | 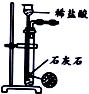 | 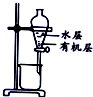 |
| 目的 | 除去Cl2中含有的少量HCl | 蒸发NaCl饱和溶液制备NaCl晶体 | 制取少量纯净的CO2气体 | 分离酒精和水的混合溶液 |
| A. | A | B. | B | C. | C | D. | D |
5.下列表示对应化学反应或过程的离子方程式正确的是( )
| A. | 铜片插入硝酸银溶液中:Cu+Ag+═Cu2++Ag | |
| B. | 碳酸氢钙与过量的NaOH溶液反应Ca2++2HCO3-+2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 用石墨作电极电解AlCl3溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$ Cl2↑+H2↑+2OH- | |
| D. | FeCl3溶液用于蚀刻印刷电路:Cu+2Fe3+═Cu2++2Fe2+ |
2.下列事实可能证明一水合氨是弱碱的是( )
| A. | 氨水能跟H2SO4反应生成(NH4)2SO4 | B. | 铵盐受热易分解 | ||
| C. | 0.1mol/L的氨水可使酚酞试液变红 | D. | 25℃,0.1mol/L氨水的pH约为12 |

 .
.
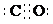 或
或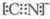 ;
;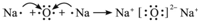 .
.