题目内容
6.(a)铁元素在人类生活中扮演着非常重要的角色,不仅仅是重要的建筑材料,也是人体必须的微量元素.每年钢铁的腐蚀带来巨大的经济损失.某校研究小组在实验室中模拟钢铁在自然环境下的腐蚀,设置如下装置(图A-C),几天后观察结果: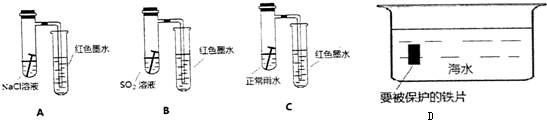
请回答下列问题:
(1)请比较以上三个装置中右侧导管中红墨水的高度:A>C>B.请写出A装置中,钢铁锈蚀时正极反应的电极反应式O2+4e-+2H2O=4OH-.
(2)钢铁的防腐有重大的意义,生活中常将金属制品放在干燥处或者涂上矿物油予以保护,现请你从电化学角度设计一种方法保护下图中钢铁以免被腐蚀,请将图D完成:
(b)下面是一种常见补铁药品说明书中的部分内容:该药品含Fe2+:33%~36%,不溶于水但能溶于人体中的胃酸,与Vc(维生素C)同服可增加本品吸收.某乙同学采用在酸性条件下用高锰酸钾标准溶液滴定的方法测定该药品是否合格,反应原理为:5Fe2++8H++MnO4-═5Fe3++Mn2++4H2O,准确称量上述药品10.00g,将其全部溶于试剂1中,配制成1000mL溶液,取出20.00mL,用0.0200mol/L的KMnO4溶液滴定,用去KMnO4溶液12.00mL.
(3)该实验中的试剂1是C(填序号).
A.蒸馏水B.稀盐酸C.稀硫酸D.稀硝酸
(4)请简述判断滴定终点的现象:当滴入最后一滴高锰酸钾溶液时,溶液变成紫红色,且30s保持不变,则到达滴定终点.
(5)请通过计算,说明该药品含铁量是否合格合格(填“合格”或“不合格”)(Fe的摩尔质量为56g/mol)
分析 (1)强酸性条件下,铁发生析氢腐蚀,中性或弱酸性条件下,铁发生吸氧腐蚀,A装置溶液呈中性,铁发生吸氧腐蚀,正极上氧气得电子发生还原反应;
(2)作原电池正极或电解池阴极的金属被保护;
(3)试剂1起溶解作用,盐酸、稀硫酸均可,但试剂2不能用盐酸,易被高锰酸钾氧化,影响实验测定,则该实验中的试剂2与甲同学设计的实验中的试剂1都可以是稀硫酸;
(4)KMnO4溶液用酸式滴定管盛放,滴定时左手旋转活塞,滴入样品溶液中,当滴入最后一滴高锰酸钾溶液时,溶液变成紫红色,且30s保持不变,则到达滴定终点;
(5)设含亚铁离子为xmol,则
5Fe2++8H++MnO4-═5Fe3++Mn2++4H2O
5 1
x 0.02mol×12×0.001L,
x=1.2×10-3mol,
1000mL溶液,取出20.00mL,则药品中含n(Fe2+)=0.0200mol/L×12.00×10-3L×5×$\frac{1000mL}{20mL}$=0.0600mol,
m(Fe2+)=0.0600mol×56g/mol=3.36g,
含“铁”量为:$\frac{3.36g}{10g}$×100%=33.6%,
依据说明书中的部分内容可知该药品含Fe2+33%~36%,判断该药品是否合格.
解答 解:(1)强酸性条件下,铁发生析氢腐蚀,中性或弱酸性条件下,铁发生吸氧腐蚀,A装置溶液呈中性,铁发生吸氧腐蚀,B、C溶液呈酸性,铁发生析氢腐蚀,但B中酸性较强,所以铁发生腐蚀严重,发生吸氧腐蚀时左边试管中压强减小,右边导管中红墨水上升,B、C右边导管中红墨水下降,且B下降比C多,所以右侧导管中红墨水高度:A>C>B;
A中铁发生吸氧腐蚀,正极上氧气得电子发生还原反应,电极反应式为O2+4e-+2H2O=4OH-,
故答案为:A>C>B;O2+4e-+2H2O=4OH-;
(2)作原电池正极或电解池阴极的金属被保护,所以Fe可以连接比铁活泼的金属或连接电源负极,即牺性阳极的阴极保护法或外加电流的阴极保护法,答:可采用牺性阳极的阴极保护法或外加电流的阴极保护法.
(3)试剂1起溶解作用,盐酸、稀硫酸均可,但试剂2不能用盐酸,易被高锰酸钾氧化,影响实验测定,则该实验中的试剂2与甲同学设计的实验中的试剂1都可以是稀硫酸,故答案为:C;
(4)KMnO4溶液用酸式滴定管盛放,滴定时左手旋转活塞,滴入样品溶液中,当滴入最后一滴高锰酸钾溶液时,溶液变成紫红色,且30s保持不变,则到达滴定终点;
故答案为:当滴入最后一滴高锰酸钾溶液时,溶液变成紫红色,且30s保持不变,则到达滴定终点;
(5)设含亚铁离子为xmol,则
5Fe2++8H++MnO4-═5Fe3++Mn2++4H2O
5 1
x 0.02mol×12×0.001L,
x=1.2×10-3mol,
1000mL溶液,取出20.00mL,则药品中含n(Fe2+)=0.0200mol/L×12.00×10-3L×5×$\frac{1000mL}{20mL}$=0.0600mol,
m(Fe2+)=0.0600mol×56g/mol=3.36g,
含“铁”量为:$\frac{3.36g}{10g}$×100%=33.6%,
说明书中的部分内容可知该药品含Fe2+33%~36%,则该药品含“铁”量合格,
故答案为:合格.
点评 本题考查金属腐蚀与防护,明确原电池原理和电解池原理即可解答,知道钢铁发生析氢腐蚀和吸氧腐蚀的条件、区别,知道防止金属被腐蚀的方法,题目难度不大.

 实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H3PO4(浓)+NaH2PO4+HBr、CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O
实验室用乙醇、浓磷酸和溴化钠反应来制备溴乙烷,其反应原理和实验的装置如下(反应需要加热,图中省去了加热装置):H3PO4(浓)+NaH2PO4+HBr、CH3CH2OH+HBr$\stackrel{△}{→}$CH3CH2Br+H2O有关数据见下表:
| 乙醇 | 溴乙烷 | 溴 | |
| 状态 | 无色 液体 | 无色 液体 | 深红棕色 液体 |
| 密度/g•cm-3 | 0.79 | 1.44 | 3.1 |
| 沸点/℃ | 78.5 | 38.4 | 59 |
(2)B中进水口为b(填“a”或“b”)口.
(3)实验中用滴液漏斗代替分液漏斗的优点为平衡压强,使浓磷酸顺利流下.
(4)制取氢溴酸时,为什么不能用浓H2SO4代替浓磷酸?2HBr+H2SO4(浓)=Br2+SO2↑+2H2O(用化学方程式表示).
(5)将C中的馏出液转入三角烧瓶中,边振荡边逐滴滴入浓H2SO4以除去水等杂质,滴加浓硫酸约1~2mL,使溶液明显分层,再用分液漏斗分去硫酸层,将经硫酸处理后的溴乙烷转入蒸馏瓶,水浴加热蒸馏,收集到35~40℃馏分约10.0g,从乙醇的角度考虑,本实验所得溴乙烷的产率是53.3%.
| A. | 摩尔是一个基本物理量,表示物质所含粒子的多少 | |
| B. | 1mol氢中含有2mol氢原子和2mol电子 | |
| C. | 1molH2O的质量等于NA个H2O质量的总和(NA表示阿伏加德罗常数) | |
| D. | 12g碳所含的原子数就是阿伏加德罗常数 |
| A. | 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,则△H<0 | |
| B. | 铁片镀锌时,铁片与外电源的正极相连 | |
| C. | 以熔融Al2O3为电解质进行电解冶炼铝,熔融体中Al3+向阳极移动 | |
| D. | t℃时,恒容密闭容器中反应:NO2(g)+SO2(g)?NO(g)+SO3(g),通入少量O2,$\frac{c(NO).c(S{O}_{3})}{c(N{O}_{2}).c(S{O}_{2})}$的值及SO2转化率不变 |



