题目内容
钠、铝、铁是三种重要的金属.请填写下列空白:
(1)将一小块金属钠投入水中,发生反应的离子方程式为 ;可观察到的实验现象是 (填序号).
①钠沉到水底 ②钠熔成小球 ③小球四处游动 ④钠浮在水面上
(2)Fe2O3与HCl在一定条件下反应,所得产物的化学式是 ,向该产物的水溶液中滴加KSCN溶液,则溶液变成 色.
(3)写出铝与NaOH溶液反应的离子方程式 .
(1)将一小块金属钠投入水中,发生反应的离子方程式为
①钠沉到水底 ②钠熔成小球 ③小球四处游动 ④钠浮在水面上
(2)Fe2O3与HCl在一定条件下反应,所得产物的化学式是
(3)写出铝与NaOH溶液反应的离子方程式
考点:常见金属元素的单质及其化合物的综合应用,钠的化学性质,铝的化学性质,铁的化学性质
专题:几种重要的金属及其化合物
分析:(1)钠和水反应生成氢氧化钠和氢气,结合钠的物理性质解答;
(2)Fe2O3与HCl在反应生成FeCl3和水;
(3)铝与NaOH溶液反应生成偏铝酸钠和氢气.
(2)Fe2O3与HCl在反应生成FeCl3和水;
(3)铝与NaOH溶液反应生成偏铝酸钠和氢气.
解答:
解:(1)钠的密度小于水的密度,所以钠能浮在水面上,钠的熔点较低,能和水剧烈反应生成氢气,所以在水中,钠能熔成小球,且四处游动,并发出嘶嘶的响声,发生的离子反应方程式为:2Na+2H2O═2Na++2OH-+H2↑,
故答案为:2Na+2H2O═2Na++2OH-+H2↑;②③④;
(2)Fe2O3与HCl在反应生成FeCl3和水,若向其中一支试管中滴加KSCN溶液,铁离子遇到硫氰酸根离子发生络合反应生成红色的络合物,
故答案为:FeCl3;红;
(3)铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,
故答案为:2Al+2H2O+2OH-═2AlO2-+3H2↑.
故答案为:2Na+2H2O═2Na++2OH-+H2↑;②③④;
(2)Fe2O3与HCl在反应生成FeCl3和水,若向其中一支试管中滴加KSCN溶液,铁离子遇到硫氰酸根离子发生络合反应生成红色的络合物,
故答案为:FeCl3;红;
(3)铝和氢氧化钠溶液反应生成偏铝酸钠和氢气,离子反应方程式为:2Al+2H2O+2OH-═2AlO2-+3H2↑,
故答案为:2Al+2H2O+2OH-═2AlO2-+3H2↑.
点评:本题综合考查金属的性质及应用,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
能用H++OH-=H2O来表示的化学反应是( )
| A、Cu(OH)2和H2SO4溶液反应 |
| B、KOH溶液和醋酸溶液反应 |
| C、澄清石灰水和HNO3溶液反应 |
| D、Ba(OH)2溶液和H2SO4溶液反应 |
在酸性溶液中,可大量共存的离子是( )
| A、K+ Na+ OH- SO42- |
| B、Mg2+ SO42- NH4+ Cl- |
| C、K+ Na+ HCO3- Cl- |
| D、Ag+ Na+ NO3- Cl- |
下列离子方程式正确的是( )
| A、实验室中制取CO2:CO32-+2H+═CO2↑+H2O |
| B、钠投入CuSO4溶液中:2Na+Cu2++2H2O═2Na++Cu(OH)2↓+H2↑ |
| C、向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O═HClO+HSO3- |
| D、向酸性KMnO4溶液中滴加双氧水:2MnO4-+H2O2+6H+═2Mn2++3O2↑+4H2O |
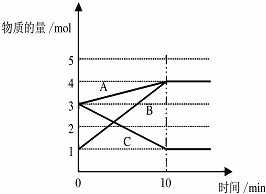 (1)将一定量的A、B、C三种物质(都是气体)放入固定体积为10L的密闭容器中,一定条件下发生反应,一段时间内测得各物质的物质的量变化如图所示.
(1)将一定量的A、B、C三种物质(都是气体)放入固定体积为10L的密闭容器中,一定条件下发生反应,一段时间内测得各物质的物质的量变化如图所示.