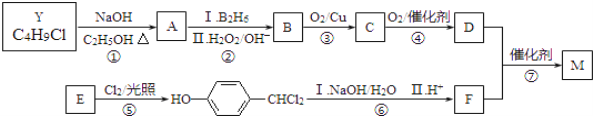
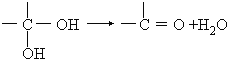
题目内容
【题目】下列说法正确的是( )
①金属和非金属化合形成离子键
②离子键是阳离子,阴离子的相互吸引
③两个非金属原子间不可能形成离子键
④非金属原子间不可能形成离子键
⑤离子化合物可能含有共价键
⑥共价化合物中可能有离子键
A. ![]() B.
B. ![]() C. ③ ⑤D.
C. ③ ⑤D. ![]()
【答案】C
【解析】
①金属和非金属化合一般形成离子键,可能形成共价键,如氯化铝中只含共价键,故错误;
②离子键是阳离子、阴离子的静电作用力,含吸引和排斥力,故错误;
③两个非金属原子间只能以共用电子对结合,则只能形成共价键,故正确;
④非金属原子间可能形成离子键,如铵盐为离子化合物,故错误;
⑤离子化合物中一定含离子键,可能含共价键,如NaOH中含离子键和共价键,故正确;
⑥共价化合物中一定不含离子键,含离子键的为离子化合物,故错误。
所以C选项是正确的。

【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a | b | c | |||||||||||||||
e | f | ||||||||||||||||
试回答下列问题:
(1)写出元素e的基态原子电子排布式________________,其未成对电子数为________。
(2)c在空气中燃烧产物的分子构型为_____,中心原子的杂化形式为______杂化。c能形成一种八元环状形同王冠的单质分子,原子的杂化形式为______杂化。
(3)b单质晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示。

若已知b的原子半径为d厘米,NA代表阿伏加德罗常数,b的相对原子质量为M,请回答:
①晶胞中b原子的配位数为_____,表示原子空间占有率的代数式为_____________。
②该晶体的密度为_____________g/cm3(用含有关字母的代数式表示)。a、f中,与单质b晶体中原子的堆积方式相同的是__________(填元素符号)。