题目内容
5.下列说法正确的是( )| A. | 因为水分子间存在氢键,所有水分子较稳定 | |
| B. | 碘固体升华过程中吸收的热量用于克服碘原子间的作用力 | |
| C. | 溴化氢溶于水能电离出H+、Br-,所以溴化氢是离子化合物 | |
| D. | 纯碱和烧碱的熔化均破坏了离子键 |
分析 A.氢键与水的稳定性无关;
B.分子晶体升华破坏分子间作用力;
C.溴化氢中只有共价键属于共价化合物;
D.离子化合物熔化破坏离子键.
解答 解:A.氢键影响水的沸点高低,与水的稳定性无关,影响稳定性的因素是共价键,故A错误;
B.碘固体属于分子晶体升华过程中吸收的热量用于克服碘分子间作用力,不能破坏原子间的作用力,故B错误;
C.溴化氢中只有共价键属于共价化合物,所以HBr不是离子化合物,故C错误;
D.离子化合物熔化破坏离子键,纯碱和烧碱均为离子化合物,所以二者熔化均破坏了离子键,故D正确.
故选D.
点评 本题考查氢键和化学键知识,题目难度不大,注意把握氢键、分子间作用力的区别和联系以及共价键、离子键等,学习中注意相关知识的理解和掌握,注意氢键对物质的性质的影响.

练习册系列答案
相关题目
15.下列实验操作、现象和结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | CH2=CH2通入溴的四氯化碳溶液中 | 溶液褪色 | CH2=CH2发生取代反应 |
| B | KIO3溶液中加入HI溶液并加入淀粉 | 溶液变蓝色 | 氧化性:KIO3>I2 |
| C | 将盛满氯气的试管倒扣在水槽中,放在日光下静置一段时间 | 气体逐渐减少,最后变为无色 | Cl2置换出水中的氧生成了O2 |
| D | 将苯、溴水混合后加入大试管加热 | 试管底部产生油状物 | 苯发生取代反应生成溴苯 |
| A. | A | B. | B | C. | C | D. | D |
13.下列说法正确的是( )
| A. | 化合物 按系统命名法的名称为3,4-二甲基戊烷 按系统命名法的名称为3,4-二甲基戊烷 | |
| B. | 淀粉和纤维素的化学式均为(C6H10O5)n,二者互为同分异构体 | |
| C. | 通常用酒精消毒,其原理是酒精使细菌中的蛋白质变性而失去生理活性 | |
| D. | 等质量的聚乙烯、甲烷、乙烯分别充分燃烧,所耗氧气的量依次减少 |
20.下列表示对应的离子方程式正确的是( )
| A. | 纯碱与醋酸反应:CO32-+2H+=H2O+CO2↑ | |
| B. | 等物质的量的SO2和Cl2通入水中:SO2+Cl2+2H2O=4H++SO42-+2Cl- | |
| C. | NH4HCO3溶液与过量的浓NaOH溶液反应:NH4++OH-=NH3↑+H2O | |
| D. | 锌与稀硝酸反应:Zn+2H+=Zn2++H2↑ |
10.对于SO2和CO2的说法中正确的是( )
| A. | 都是直线形结构 | B. | 中心原子都采用SP杂化轨道 | ||
| C. | SO2为V形结构,CO2为直线形结构 | D. | S原子和C原子上都没有孤对电子 |
17.下列物质属于分子晶体的化合物是( )
| A. | 石英 | B. | 硫磺 | C. | 干冰 | D. | 食盐 |
14.除去括号内杂质所用试剂和方法,正确的是( )
| 选项 | 物质 | 所用试剂 | 方法 |
| A. | 乙醇(乙酸) | 碳酸钠溶液 | 分液 |
| B. | 溴苯(溴) | 氢氧化钠溶液 | 蒸馏 |
| C. | 乙酸乙酯(乙酸) | 饱和碳酸钠溶液 | 过滤 |
| D. | 乙醇(水) | 生石灰 | 蒸馏 |
| A. | A | B. | B | C. | C | D. | D |
15.氰酸铵(NH4CNO)与尿素[CO(NH2)2]( )
| A. | 互为同系物 | B. | 互为同分异构体 | C. | 都是共价化合物 | D. | 都是有机化合物 |
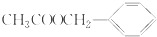 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下: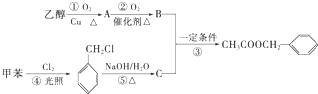
 .
.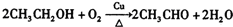 ;
;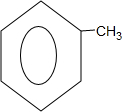 +Cl2$\stackrel{光照}{→}$
+Cl2$\stackrel{光照}{→}$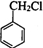 +HCl.
+HCl.