题目内容
12.今有11种物质:①铝线;②石墨;③氯气;④BaSO4晶体;⑤纯硫酸;⑥金刚石;⑦石灰水;⑧乙醇;⑨熔融的KNO3;⑩NH3;⑪盐酸.其中:(1)能导电的是(填序号,下同)①②⑦⑨⑪;
(2)属于电解质的是④⑤⑨;
(3)属于非电解质的是⑧⑩;
(4)既不是电解质又不是非电解质的是①②③⑥⑦⑪.
分析 (1)金属单质和在熔融状态下的电解质以及其溶液都能导电;
(2)电解质是指:在水溶液中或熔融状态下能够导电的化合物.电解质水溶液中或熔融状态下能够导电,是因电解质自身可以离解成自由移动的离子;单质、混合物既不是电解质也不是非电解质;
(3)非金属单质是由非金属元素组成的.一般的单质除汞和金外,带金字旁的是金属;
(4)单质与混合物既不是电解质也不是非电解质.
解答 解:①铝线是金属单质,能导电,既不是电解质也不是非电解质;
②石墨是非金属单质,能导电,既不是电解质也不是非电解质;
③氯气不能导电,是非金属单质,既不是电解质也不是非电解质;
④BaSO4晶体不能导电,熔融状态下能导电,属于电解质;
⑤纯硫酸不能导电,溶于水能导电,是电解质;
⑥金刚石是非金属单质,不能导电,既不是电解质也不是非电解质;
⑦石灰水能导电,属于混合物,既不是电解质也不是非电解质;
⑧乙醇不能导电,属于非电解质;
⑨熔融的KNO3能导电,是电解质;
⑩NH3不能导电,属于非电解质;
⑪盐酸能导电,属于混合物,既不是电解质也不是非电解质;
故答案为:(1)①②⑦⑨⑪;
(2)④⑤⑨;
(3)⑧⑩;
(4)①②③⑥⑦⑪.
点评 本题重点考查了电解质、非金属元素概念的辨析,解题时紧抓住电解质必须是化合物,以及导电是在水溶液或熔化状态下为条件,金属单质、半导体材料和电解质溶液都能导电是解答的关键,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.化学与生活密切相关,下列有关说法正确的是( )
| A. | 油脂、乙酸乙酯都属于酯类,水解后都会生成乙醇 | |
| B. | 人的皮肤在强紫外线的照射下将会失去生理活性 | |
| C. | 棉花和蚕丝的主要成分都是纤维素 | |
| D. | 制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料 |
7.下列物质在水溶液中的电离方程式正确的是( )
| A. | NaHSO4═Na++HSO4- | B. | Al2(SO4)3═2Al3++3SO42- | ||
| C. | NH4Cl═NH3+H++Cl- | D. | H2CO3═2H++CO32- |
17. Ⅰ已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)?FeO(s)+H2(g),其平衡常数为K2.在温度973K和1173K情况下,K1、K2的值分别如表:
Ⅰ已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)?FeO(s)+H2(g),其平衡常数为K2.在温度973K和1173K情况下,K1、K2的值分别如表:
(1)通过表格中的数值可以推断:反应①是吸热(填“吸热”或“放热”)反应.
(2)现有反应③:CO2(g)+H2(g)?CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学
表达式:K3=$\frac{[CO]•[{H}_{2}O]}{[{H}_{2}]•[C{O}_{2}]}$.
(3)根据反应①与②可推导出K1、K2与K3之间的关系式K3=$\frac{{K}_{1}}{{K}_{2}}$.根据此关系式及表格数据,也能推断出反应③是吸热(填“吸热”或“放热”)反应.
Ⅱ在一密闭容器中发生反应N2+3H2?2NH3△H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
(1)处于平衡状态的时间段是ACDF(填选项字母).
A.t0~t1 B.t1~t2 C.t2~t3 D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是(填选项).
A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加催化剂 F.充入氮气
t1时刻C;t4时刻B.
(3)依据(2)中的结论,下列时间段中,氨的百分含量最低的是D(填选项字母).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6.
 Ⅰ已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)?FeO(s)+H2(g),其平衡常数为K2.在温度973K和1173K情况下,K1、K2的值分别如表:
Ⅰ已知化学反应①:Fe(s)+CO2(g)?FeO(s)+CO(g),其平衡常数为K1;化学反应②:Fe(s)+H2O(g)?FeO(s)+H2(g),其平衡常数为K2.在温度973K和1173K情况下,K1、K2的值分别如表:| 温度 | K1 | K2 |
| 973K | 1.47 | 2.33 |
| 1173K | 2.15 | 1.67 |
(2)现有反应③:CO2(g)+H2(g)?CO(g)+H2O(g),请你写出该反应的平衡常数K3的数学
表达式:K3=$\frac{[CO]•[{H}_{2}O]}{[{H}_{2}]•[C{O}_{2}]}$.
(3)根据反应①与②可推导出K1、K2与K3之间的关系式K3=$\frac{{K}_{1}}{{K}_{2}}$.根据此关系式及表格数据,也能推断出反应③是吸热(填“吸热”或“放热”)反应.
Ⅱ在一密闭容器中发生反应N2+3H2?2NH3△H<0,达到平衡后,只改变某一个条件时,反应速率与反应时间的关系如图所示:回答下列问题:
(1)处于平衡状态的时间段是ACDF(填选项字母).
A.t0~t1 B.t1~t2 C.t2~t3 D.t3~t4 E.t4~t5 F.t5~t6
(2)t1、t3、t4时刻分别改变的一个条件是(填选项).
A.增大压强 B.减小压强 C.升高温度 D.降低温度 E.加催化剂 F.充入氮气
t1时刻C;t4时刻B.
(3)依据(2)中的结论,下列时间段中,氨的百分含量最低的是D(填选项字母).
A.t0~t1 B.t2~t3 C.t3~t4 D.t5~t6.
4.某物质属于电解质,则该物质不可能属于( )
| A. | 金属氧化物 | B. | 强碱 | C. | 单质 | D. | 正盐 |
17.用下列实验装置进行相应实验,装置正确且能达到实验目的是( )
| A. | 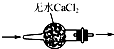 干燥SO2气体 | |
| B. |  蒸发CH3COONa溶液得醋酸钠晶体 | |
| C. |  分离有机层与水层,水层从分液漏斗下口放出 | |
| D. | 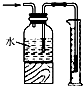 测量氯气的体积 |
18.设阿伏加德罗常数为NA,则下列说法正确的是( )
| A. | 常温常压下,11.2 L甲烷中含有的氢原子数为2NA | |
| B. | 标准状况下,0.3 mol二氧化硫中含有的氧原子数为0.3NA | |
| C. | 常温常压下,2 g H2的分子数为NA | |
| D. | 常温常压下,1 mol/L MgCl2溶液中含Cl-数为2NA |



