题目内容
【题目】利用如图装置测定中和热的实验步骤如下:
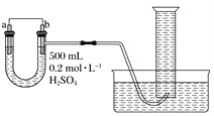
①用量筒量取50mL0.25mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50mL0.55mol/LNaOH溶液,并用另一温度计测出其温度;
③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:

(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3kJ/mol): ______;
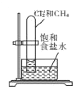
(2)学生甲用稀硫酸与稀烧碱溶液测定中和热装置如图。
①实验时所需要的玻璃仪器除烧杯、量筒外还需要:____。
②该装置中有一处错误是:_____。
(3)用相同浓度和体积的氨水(NH3·H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会____(填“偏大”、“偏小”或“无影响”)。
【答案】![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol 温度计、环形玻璃搅拌棒 大烧杯上没有盖上硬纸板 偏小
Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol 温度计、环形玻璃搅拌棒 大烧杯上没有盖上硬纸板 偏小
【解析】
(1)根据酸碱中和热的含义书写热化学方程式;
(2)①依据中和热测定实验的过程和仪器分析中和热实验时所需的玻璃仪器;
②根据所给的装置图,可知缺少硬纸板,大烧杯上如不盖硬纸板,会使一部分热量散失;
(3)NH3H2O为弱电解质,电离吸热。
(1)中和热数值为57.3 kJ/mol,反应放热,则中和热的热化学方程式:![]() H2SO4(aq)+NaOH(aq)=
H2SO4(aq)+NaOH(aq)=![]() Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol;
Na2SO4(aq)+H2O(l) ΔH=-57.3 kJ/mol;
(2)①依据量热计的结果和原理分析,测定中和热实验时所需的玻璃仪器有烧杯、量筒、温度计、环形玻璃搅拌棒,
故答案为:温度计、环形玻璃搅拌棒;
②实验装置保温、隔热效果必须好,否则影响实验结果,所以装置缺少硬纸板,故答案为:大烧杯上没有盖上硬纸板;
(3)NH3H2O为弱碱,电离过程为吸热过程,用相同浓度和体积的氨水(NH3H2O)代替NaOH溶液进行上述实验,测得的中和热的数值偏小;
故答案为:偏小。

 期末100分闯关海淀考王系列答案
期末100分闯关海淀考王系列答案 小学能力测试卷系列答案
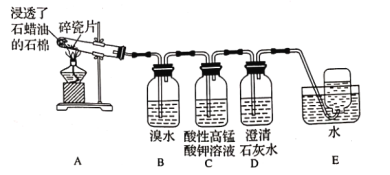
小学能力测试卷系列答案【题目】下述实验方案能达到实验结果的是( )
编号 | A | B | C | D |
实验方案 |
|
片刻后在 |
|
置于光亮处 |
实验结果 | 铁钉发生析氢反应 |
| 左球气体颜色加深; 右球气体颜色变浅 | 甲烷与氯气发生加成反应 |
A.AB.BC.CD.D