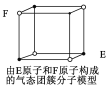
��Ŀ����
����Ŀ��(1)��֪��Ӧ2HI(g)=H2(g)+I2(g)�ġ�H=+11kJ��mol-1��1molH2(g)��1molI2(g)�����л�ѧ������ʱ�ֱ���Ҫ����436kJ��151kJ����������1molHI(g)�����л�ѧ������ʱ�����յ�����Ϊ______________kJ��
(2)��֪ij�ܱ������д�������ƽ�⣺CO(g)+H2O(g)![]() CO2(g)+H2(g)��CO��ƽ�����ʵ���Ũ��c(CO)���¶�T�Ĺ�ϵ��ͼ��ʾ��
CO2(g)+H2(g)��CO��ƽ�����ʵ���Ũ��c(CO)���¶�T�Ĺ�ϵ��ͼ��ʾ��
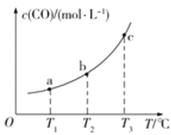
�ٸ÷�Ӧ��H_____________0(����������������)
����T1��T2ʱ��ƽ�ⳣ���ֱ�ΪK1��K2����K1_____________K2(��������������������=��)��
(3)�ں����ܱ������У�����������MoS2��O2����������Ӧ��2MoS2(s)+7O2(g)![]() 2MoO3(s)+4SO2(g)��H�����������ƽ��ת��������ʼѹǿ���¶ȵĹ�ϵ��ͼ��ʾ��
2MoO3(s)+4SO2(g)��H�����������ƽ��ת��������ʼѹǿ���¶ȵĹ�ϵ��ͼ��ʾ��
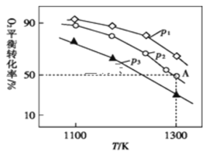
��p1��p2��p3�Ĵ�С��___________��
������ʼʱͨ��7.0molO2��p2Ϊ7.0kPa����A��ƽ�ⳣ��Kp=___________(������ƽ���ѹ��������ƽ��Ũ�ȼ��㣬��ѹ=��ѹ����������ʵ���������д������ʽ����)��
(4)�п�Ժ���ݻ�ѧ�����о�����Fe3(CO)12/ZSM-5��CO2����ϳɵ�̼ϩ����Ӧ�����ò��ﺬCH4��C3H6��C4H8�ȸ������Ӧ������ͼ��
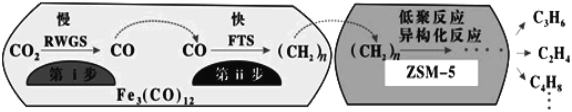
����������Na��K��Cu������(����Ҳ�������)�ɸı䷴Ӧ��ѡ���ԣ�������������ͬʱ�����Ӳ�ͬ������������ͬʱ�����CO2ת���ʺ���������ʵ������������
���� | CO2ת����(%) | �����������в����е�ռ��(%) | ||
C2H4 | C3H6 | ���� | ||
Na | 42.5 | 35.9 | 39.6 | 24.5 |
K | 27.2 | 75.6 | 22.8 | 1.6 |
Cu | 9.8 | 80.7 | 12.5 | 6.8 |
������ߵ�λʱ������ϩ�IJ�������Fe3(CO)12/ZSM-5������_______����Ч����ã�������������ߵ�λʱ������ϩ�����ĸ���ԭ����:___________
������˵����ȷ����______��
a���������ķ�ӦΪ��CO2+H2![]() CO+H2O
CO+H2O
b����������Ӧ�Ļ�ܵ��ڵ�����
c������������Ҫ�ڵ;۷�Ӧ���칹����Ӧ����������
d��Fe3(CO)12/ZSM-5ʹCO2����ϳɵ�̼ϩ������H��С
e�����Ӳ�ͬ������Ӧ��ƽ�ⳣ��������ͬ
���𰸡�299 < > p1>p2>p3 ![]() K ����������ϩ�ķ�Ӧ����Ҫ�Ļ�ܣ��ӿ���ϩ�������ʣ�������������Ӧ������Ӱ�� ac
K ����������ϩ�ķ�Ӧ����Ҫ�Ļ�ܣ��ӿ���ϩ�������ʣ�������������Ӧ������Ӱ�� ac
��������
(1)�ʱ�=��Ӧ��ļ���֮��-������ļ���֮�ͣ���1molHI(g)�����л�ѧ������ʱ�����յ�����Ϊx����2x -436kJ/mol-151kJ/mol=11kJ/mol�����x=299 kJ/mol��
(2)�پ�ͼ��֪���¶����ߣ�CO��ƽ��Ũ������˵�������¶�ƽ�������ƶ����÷�Ӧ������ӦΪ���ȷ�Ӧ�����ԡ�H<0��
�ڶ��ڷ��ȷ�Ӧ���¶�Խ�ߣ�ƽ�ⳣ��ԽС��T1<T2����K1>K2��
(3)�ٸ÷�ӦΪ��������ʵ������ٵķ�Ӧ�������¶���ͬʱ��ѹǿԽ��������ƽ��ת����Խ������p1>p2>p3��
�ڳ�ʼͶ��Ϊ7.0molO2��ƽ��ʱO2��ת����Ϊ50%������n(O2)=3.5mol�����ݷ�Ӧ����ʽ��֪ƽ��ʱn(SO2)=2mol��n(O2)=7mol-3.5mol=3.5mo�����������������ѹǿ֮�ȵ�����������ʵ���֮�ȣ���ʼ������������ʵ���Ϊ7mol��ѹǿΪ7.0kPa����ƽ��ʱp(O2)=3.5kPa��p(SO2)=2kPa��Kp=![]()
![]() ��
��
(4)���ɱ������ݿ�֪������ΪNaʱ����������Ӧռ�ȴ�����ΪCuʱ��CO2ת���ʵͣ������ϩ�IJ��ʡ�CO2ת���ʺͶԸ���Ӧ��Ӱ�죬ѡ������K����Ч����ã���������ߵ�λʱ������ϩ������������������Ӧռ���٣������������Խ���������ϩ�ķ�Ӧ����Ҫ�Ļ�ܣ��ӿ���ϩ�������ʣ�������������Ӧ������Ӱ�죻
��a���ɴ�CO2����ϳɵ�̼ϩ����Ӧ��֪������������ӦΪ��CO2+H2CO+H2O����a��ȷ��
b����������Ӧ������Ӧ���������ǿ췴Ӧ����Ӧ�Ļ��Խ�ͣ���Ӧ����Խ�죬���Ե�������Ӧ�Ļ�ܸ��ڵ���������b����
c�������ɸı䷴Ӧ��ѡ���ԣ����Դ���������Ҫ�ڵ;۷�Ӧ���칹����Ӧ���������ã���c��ȷ��
d���������ܸı�ƽ��״̬�����ܸı��ʱ䣬��d����
e����Ӧ��ƽ�ⳣ��ֻ���¶��йأ��¶Ȳ���ƽ�ⳣ�����䣬�����ӵ������أ���e����
��������ѡac��

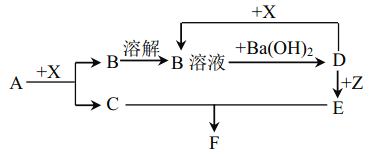
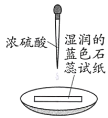
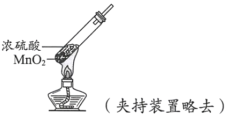
����Ŀ����������ʵ�鷽���������Ũ���������������жϺ�������
ʵ�鷽�� | ʵ��I�� | ʵ��II�� |
ʵ������ | ��ֽ���������ڣ���Ե��� | ��ɫ�����ܽ⣬��Һ�ӽ���ɫ(��Һ����Ԫ�ؽ��� |
A.��I��֪��Ũ���������ˮ��B.��I��֪��Ũ�������������
C.��II��֪��Ũ�������ǿ������D.��II��֪��Ũ���������ˮ��
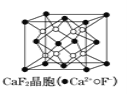
����Ŀ����֪��ѧƽ�⡢����ƽ�⡢ˮ��ƽ����ܽ�ƽ���������������ԭ������ش��������⣺
��1�����淴ӦFeO(s)��CO(g)![]() Fe(s)��CO2(g)��������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
Fe(s)��CO2(g)��������ҵ��һ����Ҫ��Ӧ�����¶���ƽ�ⳣ��K�Ĺ�ϵ���±���
T/K | 938 | 1 100 |
K | 0.68 | 0.40 |
���÷�Ӧ������̶����ܱ������н��У���һ�������´ﵽƽ��״̬���������¶ȣ���������ƽ����Է�������__�����뺤�������������ܶ�__(��������������С������������)��
��2��830�棬��ӦCO2(g)��3H2(g)![]() CH3OH(g)��H2O(g)��ƽ�ⳣ��K=1����2L���ݷ�Ӧ���з���������Ӧ���ֱ����3molCO2��2molH2��1molCH3OH��4molH2O(g)����Ӧ��__������С�������������桱���ƶ�����
CH3OH(g)��H2O(g)��ƽ�ⳣ��K=1����2L���ݷ�Ӧ���з���������Ӧ���ֱ����3molCO2��2molH2��1molCH3OH��4molH2O(g)����Ӧ��__������С�������������桱���ƶ�����
��3��25��ʱ���������ʵĵ���ƽ�ⳣ�������ʾ��
��ѧʽ | CH3COOH | NH3��H2O | H2CO3 | H2SO3 |
����ƽ�ⳣ�� | 1.7��10-5 | 1.7��10-5 | K1��4.3��10-7 K2��5.6��10-11 | K1��1.3��10-2 K2��6.3��10-8 |
��д��CH3COOH�ĵ��뷽��ʽ____�������ƽ�ⳣ������ʽK a=___��
�ڸ��ݱ��������жϣ�Ũ�Ⱦ�Ϊ0.01mol��L-1�������������ʵ���Һ�У�������ǿ����___(����)�������и���Һ�ֱ�ϡ��100����pH�仯��С����___(����)��
A��CH3COOH B��H2CO3 C��H2SO3