题目内容
2.如图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质被略去.常温常压下,A为无色有毒气体,B为红棕色粉末,C、E为金属单质.反应①、②均为工业上的重要反应.
请回答下列问题:
(1)G是NaHCO3,K是FeCl3(填化学式)
(2)C的原子结构示意图为
 .
.(3)写出H与Cl2反应生成K的离子方程式:2Fe2++Cl2═2Fe3++2Cl-.
(4)写出D与J的稀溶液反应生成G的离子方程式:CO2+CO32-+H2O=2HCO3-.
分析 B为红棕色粉末,应为Fe2O3,A为无色有毒气体,结合转化关系,可推知A具有还原性,故A为CO,则D为CO2,E为Fe;顺推可知G为NaHCO3,J为Na2CO3,H是FeCl2,K为FeCl3,金属C与氧化铁反应生成Fe与F,F为金属氧化物,既与盐酸反应又能与氢氧化钠反应,F应为Al2O3,则C是Al,I为AlCl3,L为NaAlO2,据此分析解答.
解答 解:B为红棕色粉末,应为Fe2O3,A为无色有毒气体,结合转化关系,可推知A具有还原性,故A为CO,则D为CO2,E为Fe;顺推可知G为NaHCO3,J为Na2CO3,H是FeCl2,K为FeCl3,金属C与氧化铁反应生成Fe与F,F为金属氧化物,既与盐酸反应又能与氢氧化钠反应,F应为Al2O3,则C是Al,I为AlCl3,L为NaAlO2,
(1)通过以上分析知,G是NaHCO3、K是FeCl3,故答案为:NaHCO3;FeCl3;
(2)C是Al,Al原子核外有3个电子层、最外层电子数是3,其原子结构示意图为 ,故答案为:
,故答案为: ;
;
(3)H→K的反应是亚铁离子被氯气氧化为三价铁离子,离子方程式为2Fe2++Cl2═2Fe3++2Cl-,故答案为:2Fe2++Cl2═2Fe3++2Cl-;
(4)二氧化碳与碳酸钠稀溶液反应生成生成碳酸氢钠,反应离子方程式为:CO2+CO32-+H2O=2HCO3-,故答案为:CO2+CO32-+H2O=2HCO3-.
点评 本题考查无机物的推断,本题注意以A、B为该题的突破口进行推断,注意把握相关物质的性质,熟练掌握特殊物质的颜色及性质,题目难度不大.

练习册系列答案
相关题目
14.下列叙述不正确的是( )
| A. | 常温常压下,3.2gO2所含的原子数为0.2NA | |
| B. | 标准状况下,18gH2O所含的氧原子数目为NA | |
| C. | 常温常压下,92gNO2和N2O4的混合气体中含有的原子总数为6NA | |
| D. | 标准状况下,22.4L氦气与22.4L氟气所含原子数均为2NA |
7.下列物质的性质,属于化学性质的是( )
| A. | 活性炭的吸附性 | B. | 石墨的导电性 | C. | 碳酸的不稳定性 | D. | 汽油的挥发性 |
14.下列物质的化学式书写正确是( )
| A. | 氯化钠( ClNa ) | B. | 高锰酸钾(K2MnO4) | C. | 硫酸钠(Na2S) | D. | 碳酸(H2CO3) |
11.美国加州爱德华空军基地的空军研究室,研究高能材料的化学家宣布合成并表征了一种含有N5+离子的盐类,该阳离子可看作是100多年来第三次可分离获得的全氮物种,下列有关N5+离子的叙述不正确的是( )
| A. | 它是一种阳离子 | B. | 该离子所含质子总数比电子总数多 | ||
| C. | 一个N5+离子中有36个质子 | D. | N5+离子中含有34个电子 |


 .
. .
. (或
(或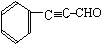 ).
). 、
、 、
、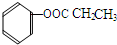 、
、 、
、 、
、 (写结构简式).
(写结构简式).