题目内容
17.银铜合金广泛应用于航空工业.从切割废料中回收银并制备铜的化工产品工艺如下: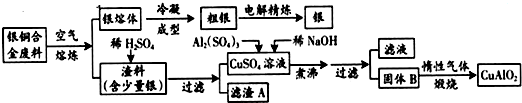
(注:Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃)
(1)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学方程式为2NO+O2=2NO2.
(2)固体混合物B的组成为Al(OH)3和CuO;在生成固体B的过程中,需控制NaOH的加入量,若NaOH过量,则因过量引起的反应的离子方程式为Al(OH)3+OH-=AlO2-+2H2O.
(3)若银铜合金中铜的质量分数为63.5%,理论上5.0kg废料中的铜可完全转化为50.0mol CuAlO2(Cu 的相对原子量取63.5),至少需要1.0mol•L-1的Al2(SO4)3溶液25.0L.
分析 由工艺流程图可知,废料在空气中熔炼时,Cu被氧化,滤渣中含有CuO及少量Ag,向滤渣中加入硫酸进行酸浸,CuO与硫酸反应,过滤得到硫酸铜溶液(含有硫酸),滤渣A为Ag;向滤液中加入硫酸铝、氢氧化钠,得到氢氧化铝、氢氧化铜,灼烧中会得到CuO、Al2O3,二者反应得到CuAlO2.
(1)无色的NO在常温下与空气中的O2迅速化合生成红棕色N02;
(2)未煮沸之前是Cu(OH)2和Al(OH)3,根据Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃判断产物;根据氢氧化铝显两性能与碱反应;
(3)根据铜元素守恒建立关系式:Cu~CuAlO2来计算;根据铝元素守恒建立关系式:Al2(SO4)3~2CuAlO2来计算.
解答 解:(1)无色的NO在常温下与空气中的O2迅速化合生成红棕色N02:2NO+O2=2NO2,红棕色气体溶于水生成硝酸和一氧化氮,故答案为:2NO+O2=2NO2;
(2)未煮沸之前是Cu(OH)2和Al(OH)3,Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃,煮沸后Cu(OH)2分解产生氧化铜,可知B为Al(OH)3和CuO;氢氧化铝显两性能与碱反应:Al(OH)3+NaOH=NaAlO2+2H2O;
故答案为:Al(OH)3和CuO;Al(OH)3+OH-=AlO2-+2H2O;
(3)由关系式:Cu~CuAlO2得n(CuAlO2)=$\frac{5000g×64%}{64g/mol}$=50.0mol,则CuAlO2为50.0mol,
由关系式:Al2(SO4)3~2CuAlO2得Al2(SO4)3=n(CuAlO2)×$\frac{1}{2}$=25.0mol,所以需要体积为 $\frac{25.0L}{1.0mol/L}$=25.0L,
故答案为:50.0,25.0.
点评 本题以从废料中回收银并制备铜化工产品为背景,考查了电解原理、沉淀的判断、氧化还原反应的配平以及化学计算,难度中等.

 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案| 选项 | ① | ② | ③ | 实验结论 |  |
| A | 浓盐酸 | MnO2 | NaOH | 制氯气并吸收尾气 | |
| B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 | |
| C | 稀盐酸 | Na2SO3 | Ba(NO3)2溶液 | SO2与可溶性钡盐均可生成白色沉淀 | |
| D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 酸性:硝酸>碳酸>硅酸 |
| A. | A | B. | B | C. | C | D. | D |
| A. | BaCl2 Na2CO3 AgNO3 盐酸 | B. | BaCl2 Na2CO3 盐酸 AgNO3 | ||
| C. | Na2CO3 盐酸 AgNO3 BaCl2 | D. | AgNO3 盐酸 BaCl2 Na2CO3 |
| A. | 1:2 | B. | 3:1 | C. | 1:1 | D. | 1:3 |
部分物质的溶解性
| NO3- | SO42- | CO32- | |
| Na+ | 溶 | 溶 | 溶 |
| Cu2+ | 溶 | 溶 | - |
| Ag+ | 溶 | 微 | 不 |
②向①的三支试管中分别加入稀盐酸,发现X的溶液中产生白色沉淀,Y的溶液中有无色无味的气体逸出.
根据①②实验现象回答下列问题:
(1)写出X、Y、Z的化学式:XAgN03 YNa2CO3 ZCuSO4
(2)写出稀盐酸与X反应的离子方程式Ag++Cl-═AgCl↓.
(3)写出Z与Ba(OH)2溶液反应的离子方程式Cu2++SO42-+Ba2++2OH-═Cu(OH)2↓+BaSO4↓.
| A. |  制取并收集二氧化碳 | B. |  铁丝字氧气中燃烧 | ||
| C. |  加热高锰酸钾制氧气 | D. |  倾倒液体 |
| A. | 一氧化碳和氢气的混和气 | |
| B. | 碳在氧气中不完全燃烧得到的混和气 | |
| C. | 电解水正极与负极气体形成的混和气 | |
| D. | 氮气和氧气的混和气 |
 .
.