题目内容
11.美国加州爱德华空军基地的空军研究室,研究高能材料的化学家宣布合成并表征了一种含有N5+离子的盐类,该阳离子可看作是100多年来第三次可分离获得的全氮物种,下列有关N5+离子的叙述不正确的是( )| A. | 它是一种阳离子 | B. | 该离子所含质子总数比电子总数多 | ||
| C. | 一个N5+离子中有36个质子 | D. | N5+离子中含有34个电子 |
分析 A、该微粒为阳离子;
B、阳离子的电子数等于质子数减去电荷数;
C、N的质子数为7,微粒中含有5个氮原子;
D、粒子的电子数等于质子数减去电荷数分析.
解答 解:A、由N5+可知,该微粒是由5个氮原子构成的阳离子,故A正确;
B、N5+的质子数为7×5=35,则电子数为35-1=34,离子所含质子总数比电子总数多,故B正确;
C、N5+的质子数为7×5=35,故C错误;
D、N5+的质子数为7×5=35,电子数为35-1=34,故D正确;
故选C.
点评 本题属于信息习题,学生应抓住信息中爆炸性的高能N5+阳离子是解答本题的关键,并注意结合所学知识来解答,注重基础,难度不大.

练习册系列答案
相关题目
3. 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完成反应(已知反应过程放热),ClO-和ClO3-的物质的量(n)与反应时间(t)的变换关系如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完成反应(已知反应过程放热),ClO-和ClO3-的物质的量(n)与反应时间(t)的变换关系如图所示.下列说法不正确的是( )
 将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完成反应(已知反应过程放热),ClO-和ClO3-的物质的量(n)与反应时间(t)的变换关系如图所示.下列说法不正确的是( )
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完成反应(已知反应过程放热),ClO-和ClO3-的物质的量(n)与反应时间(t)的变换关系如图所示.下列说法不正确的是( )| A. | Cl2和苛性钾溶液在不同温度下可能发生不同反应 | |
| B. | t1时刻,c(Cl-):c(ClO-)=5:1 | |
| C. | 原苛性钾溶液中KOH的物质的量为0.3mol | |
| D. | t2时刻,n(还原产物):n(氧化产物)=7:3 |
19.下列实验现象描述不正确的是( )
| A. | 铁丝在氧气中燃烧生成黑色固体物质 | |
| B. | 给水通直流电一段时间,正极和负极的气体体积比为2:1 | |
| C. | 二氧化碳通入紫色石蕊试液,紫色石蕊试液变成红色 | |
| D. | 红磷在空气中燃烧,产生大量白烟 |
6.“安全生产,人命关天”.国家对易燃、易爆物的生产、贮存、运输、使用有严格规定,绝不允许违章操作.下列混合物,遇明火可能发生爆炸的是( )
| A. | 一氧化碳和氢气的混和气 | |
| B. | 碳在氧气中不完全燃烧得到的混和气 | |
| C. | 电解水正极与负极气体形成的混和气 | |
| D. | 氮气和氧气的混和气 |
16.可以一次性将空气、氧气、氢气、二氧化碳区别开的最好方法是( )
| A. | 分别加入适量澄清石灰水 | B. | 分别滴加紫色石蕊试液 | ||
| C. | 分别将带火星的木条伸入瓶中 | D. | 分别将燃着的木条伸入瓶中 |
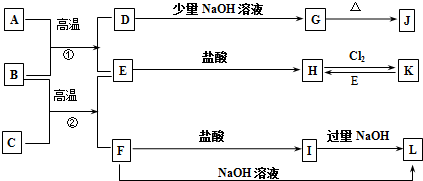
 .
.





 氧气扩散至电极表面
氧气扩散至电极表面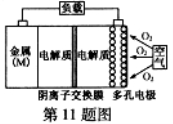 B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高
B.比较Mg、Al、Zn三种金属–空气电池,Al–空气电池的理论比能量最高