题目内容
13.已知A、B、C、D、E、F是含有同一种元素的化合物,其中F是能使红色湿润石蕊试纸变蓝的气体,它们之间能发生如下反应①A+H2O→B+C ②C+F→D
③D+NaOH$\stackrel{△}{→}$F+E+H2O
(1)写出它们的化学式:CHNO3、DNH4NO3、ENaNO3.
(2)写出各步反应的离子方程式
①3NO2+H2O═2H++2NO3-+NO,
③NH4++OH-$\frac{\underline{\;△\;}}{\;}$NH3↑+H2O.
(3)工业生产C的过程中有如下一步反应,即F经催化氧化生成B和H2O,写出该步反应的化学方程式
4NH3+5O2$\frac{\underline{\;催化剂\;}}{△}$ 4NO+6H2O.
分析 A、B、C、D、E、F是含有同一种元素的化合物,F经催化氧化生成B和H2O,则F是NH3,它们之间能发生如下反应:③D+NaOH→F+E+H2O,说明D是铵盐,E为钠盐,且A、B、C、D、E、F是含有同一种元素的化合物,则E是NaNO3,D是NH4NO3,根据②C+F→D知,C是HNO3,根据①A+H2O→B+C知,且A和B、C都含有同一种元素,则A是NO2,B是NO,根据物质的性质分析解答.
解答 解:A、B、C、D、E、F是含有同一种元素的化合物,F经催化氧化生成B和H2O,则F是NH3,它们之间能发生如下反应:③D+NaOH→F+E+H2O,说明D是铵盐,E为钠盐,且A、B、C、D、E、F是含有同一种元素的化合物,则E是NaNO3,D是NH4NO3,根据②C+F→D知,C是HNO3,根据①A+H2O→B+C知,且A和B、C都含有同一种元素,则A是NO2,B是NO,
(1)由上分析C为HNO3,D为NH4NO3,E为NaNO3,故答案为:HNO3;NH4NO3;NaNO3;
(2)①二氧化氮和水反应生成一氧化氮和硝酸,化学方程式为:3NO2+H2O=2H++2NO3-+NO,故答案为:3NO2+H2O=2H++2NO3-+NO;
②为硝酸铵与氢氧化钠反应,离子方程式为NH4++OH-$\frac{\underline{\;△\;}}{\;}$NH3↑+H2O,故答案为:NH4++OH-$\frac{\underline{\;△\;}}{\;}$NH3↑+H2O;
(3)即NH3经催化氧化生成NO和H2O,反应方程式为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
点评 本题以N元素为载体考查了含氮化合物的推断,以F为突破口结合物质间的转化分析推断,难度不大,注意多总结归纳基础知识,知道常见物质的性质.

| A. | 14g聚丙烯中含C-H键总数目为2NA | |
| B. | 1molFe与足量的稀硝酸反应转移电子总数目为2NA | |
| C. | 标准状况下,44.8L乙醛中含乙醛分子总数目为2NA | |
| D. | 常温常压下,200g质量分数为17%H2O2溶液中含氧原子总数目为2NA |
| A. | HClO4、H2SO4、H3PO4的酸性依次增强 | |
| B. | HCl、HBr、HI的稳定性依次增强 | |
| C. | 钠、镁、铝的还原性依次减弱 | |
| D. | P、S、Cl最高正价依次降低 |
①H、2H、3H为三种不同的核素;
②H、2H、3H互为同位素;
③H、2H、3H互为同素异形体;
④114号元素位于周期表第七周期VA族;
⑤氢元素质量数为1;
⑥同位素的“同位”指核素的质子数相同,在元素周期表中占相同的位置;
⑦互为同位素的原子物理性质、化学性质均相同.
| A. | ①②⑥⑦ | B. | ①②③⑥ | C. | ①②⑥ | D. | ①②③⑥⑦ |
| A. | N、P、As的电负性随原子序数的增大而增大 | |
| B. | 价电子排布为4s24p3的元素位于第四周期第ⅤA族,是p区元素 | |
| C. | 2p和3p轨道形状均为纺锤形,能量也相等 | |
| D. | 氮原子的最外层电子的轨道表示式: |
| A. | Be.C.B | B. | Li.O.Cl | C. | S.Si.Al | D. | C.S.Mg |
| A. | AlN可通过反应Al2O3+N2+3C$\frac{\underline{\;高温\;}}{\;}$2AlN+3CO合成.该反应中,每生成1 mol AlN需转移1.5 mol电子 | |
| B. | CsICl2是一种碱金属的多卤化物,这类物质在化学反应中既可表现氧化性又可表现还原性,则在CsICl2溶液中通入Cl2,有单质碘生成 | |
| C. | 反应A+3B═2C+2D在四种不同情况下的反应速率分别为①v(A)=0.15 mol/(L•s);②v(B)=0.6 mol/(L•s);③v(C)=0.4 mol/(L•s);④v(D)=0.45 mol/(L•s).该反应进行的快慢顺序为④>③=②>① | |
| D. | AlCl3溶液中加入过量稀氨水,则反应的离子方程式为:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
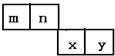 m、n、x、y四种主族元素在周期表里的相对位置如图所示.已知它们的原子序数总和为46,则:
m、n、x、y四种主族元素在周期表里的相对位置如图所示.已知它们的原子序数总和为46,则: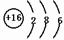 .
.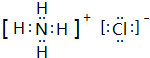 ,此物质在固态时属于离子晶体.
,此物质在固态时属于离子晶体.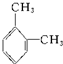 名称:邻二甲苯或1,2-二甲基苯
名称:邻二甲苯或1,2-二甲基苯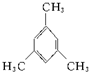 名称:1,3,5-三甲基苯.
名称:1,3,5-三甲基苯.