题目内容
【题目】实验室用下述装置制取氯气,并用氯气进行下列实验。看图回答下列问题:

(1)A、B两仪器的名称:A________,B________。
(2)写出实验室制氯气的化学方程式,并用单线桥法表示上述反应电子转移的方向和数目_____________。
(3)洗气装置C是为了除去Cl2中的HCl气体,D是为了干燥Cl2,则C、D中应分别放入的试剂是C______________,D______________。
(4)P为尾气吸收装置,写出实验室吸收氯气的反应的离子方程式_______________。
(5)ClO2具有很强的氧化性,因此常被用作消毒剂,其消毒的效率(以单位质量得到的电子数表示)是Cl2的________倍。
【答案】分液漏斗 圆底烧瓶 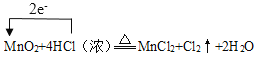 饱和食盐水 浓H2SO4 Cl2+2OH-=Cl-+ ClO-+ H2O 2.63
饱和食盐水 浓H2SO4 Cl2+2OH-=Cl-+ ClO-+ H2O 2.63
【解析】
(1)根据装置图中仪器作用和图形写出名称;(2)实验室用加热二氧化锰与浓盐酸的混合物制取氯气,反应中锰元素化合价由+4降低为+2,氯元素化合价由-1升高为0;(3)从发生装置出来的氯气中含有杂质HCl和水蒸气,可以通过盛有饱和食盐水的洗气瓶除去HCl,通过盛有浓硫酸的洗气瓶除去氯气中的水蒸气; (4)实验室用氢氧化钠溶液吸收氯气;(5)![]() 转移电子数为5,
转移电子数为5,![]() 转移电子数为2。
转移电子数为2。
(1)装置图是利用分液漏斗向圆底烧瓶中加入浓盐酸加热生成氯气的发生装置,A是分液漏斗,B是圆底烧瓶;(2)实验室用加热二氧化锰与浓盐酸的混合物制取氯气,反应方程式是![]() ,反应中锰元素化合价由+4降低为+2,氯元素化合价由-1升高为0,单线桥法表示上述反应电子转移的方向和数目为
,反应中锰元素化合价由+4降低为+2,氯元素化合价由-1升高为0,单线桥法表示上述反应电子转移的方向和数目为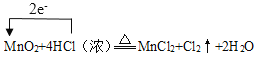 ;(3)从发生装置出来的氯气中含有杂质HCl和水蒸气,可以通过盛有饱和食盐水的洗气瓶除去HCl,通过盛有浓硫酸的洗气瓶除去氯气中的水蒸气,则中C盛放饱和食盐水、D中盛放浓硫酸; (4)实验室用氢氧化钠溶液吸收氯气,反应生成次氯酸钠、氯化钠和水,反应离子方程式是Cl2+2OH-=Cl-+ ClO-+ H2O;(5)设ClO2、 Cl2的质量都是mg,物质的量分别是
;(3)从发生装置出来的氯气中含有杂质HCl和水蒸气,可以通过盛有饱和食盐水的洗气瓶除去HCl,通过盛有浓硫酸的洗气瓶除去氯气中的水蒸气,则中C盛放饱和食盐水、D中盛放浓硫酸; (4)实验室用氢氧化钠溶液吸收氯气,反应生成次氯酸钠、氯化钠和水,反应离子方程式是Cl2+2OH-=Cl-+ ClO-+ H2O;(5)设ClO2、 Cl2的质量都是mg,物质的量分别是![]() 、
、![]() ,
,![]() 转移电子数为5,
转移电子数为5,![]() 转移电子数为2,所以转移电子数比为
转移电子数为2,所以转移电子数比为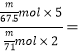 2.63 。
2.63 。