题目内容
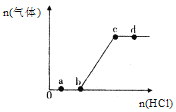
【题目】向Na2CO3、NaHCO3混合溶液中逐滴加入稀盐酸,生成气体的量随盐酸加入量的变化关系如图所示。则下列离子组在对应的溶液中一定能大量共存的是( )
A. a点对应的溶液中:Na+、OH-、SO42-、NO3-
B. b点对应的溶液中:H+、Fe3+、MnO4-、Cl-
C. d点对应的溶液中:S2-、NO3-、Fe2+、Ag+
D. c点对应的溶液中:Na+、Ca2+、NO3-、Cl-
【答案】D
【解析】
Na2CO3、NaHCO3中滴加盐酸,依次发生的反应有Na2CO3+HCl=NaCl+ NaHCO3、NaHCO3+HCl=NaCl+CO2![]() +H2O。
+H2O。
a点对应的溶液中含有HCO3-,HCO3-与OH-反应生成CO32-,所以a点对应的溶液中不能含大量OH-,故不选A;b点对应的溶液中含有HCO3-,HCO3-与H+反应生成二氧化碳气体,所以b点对应的溶液中不能含大量H+,故不选B;S2-与Fe2+、Ag+不能大量共存,d点对应的溶液为氯化钠和稀盐酸的混合溶液,NO3-、Fe2+与氢离子能发生氧化还原反应,d点对应的溶液中含有Cl-,Cl-与Ag+生成氯化银沉淀,d点对应的溶液中不能含有Ag+,故不选C;c点对应的溶液中含NaCl, NaCl与Ca2+、NO3-、Cl-不反应,故选D。

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目


