题目内容
1.可逆反应2NO2?2NO+O2在恒容密闭容器中进行,下列情况达到平衡状态的是( )①单位时间内生成nmolO2的同时生成2nmolNO2
②混合气体的平均相对分子质量不再改变
③NO2、NO、O2的反应速率之比为2:2:1
④混合气体的颜色不再改变
⑤混合气体的密度不再改变.
| A. | ①②④ | B. | ②③⑤ | C. | ①②⑤ | D. | ②④⑤ |
分析 反应达到平衡状态时,正逆反应速率相等,平衡时各种物质的物质的量、浓度等不再发生变化,可由此进行判断.
解答 解:①单位时间内生成n mol O2的同时生成2n mol NO2,生成nmol氧气会消耗2nmol二氧化氮,说明了正逆反应速率相等,达到了平衡状态,故①正确;
②混合气体的平均相对分子质量不再改变的状态,反应方程式两边气体的物质的量不同,气体的质量固定,所以平均相对分子质量不再改变,说明达到了平衡状态,故②正确;
③用NO2、NO、O2的物质的量浓度变化表示的反应速率的比为2:2:1的状态,各组分的浓度大小关系,不能说明各组分的浓度是否变化,正逆反应速率是否相等,故③错误;
④混合气体的颜色不再改变,说明二氧化氮的浓度不再变化,达到了平衡状态,故④正确;
⑤混合气体的密度不再改变的状态,由于反应两边都是气体,容器的体积不变,所以反应中密度始终不变,即密度不能作为判断化学平衡的依据,故⑤错误;
所以正确的有①②④,
故选A.
点评 本题考查化学平衡状态的判断,注意分析时要从化学方程式的反应特征判断,平衡状态的本质时正逆反应速率相等.

练习册系列答案
相关题目
11.下列制备和收集气体的实验装置合理的是( )
| A. | 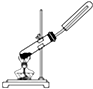 用氯化铵和氢氧化钠固体制NH3 | B. | 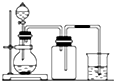 用铜片和稀硝酸制NO | ||
| C. | 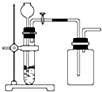 用锌粒和稀硫酸制H2 | D. | 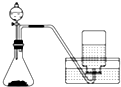 用H2O2和MnO2制O2 |
12.利用下列实验装置能完成相应实验的是( )
| A. | 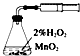 装置测定化学反应速率 | B. | 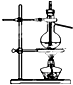 装置模拟海水蒸馏 | ||
| C. | 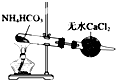 装置制备纯净的NH3 | D. |  装置比较MnO2、Cl2、S的氧化性 |
9.实验室用纯溴和苯在铁离子催化下反应制取溴苯,得到粗溴苯后,要用如下操作精制,正确的操作顺序是
①蒸馏 ②水洗分液 ③用干燥剂干燥 ④10%NaOH溶液洗分液( )
①蒸馏 ②水洗分液 ③用干燥剂干燥 ④10%NaOH溶液洗分液( )
| A. | ①②③④② | B. | ②④②③① | C. | ④②③①② | D. | ②④①②③ |
6.表示下列反应的离子方程式中,正确的是( )
| A. | 烧碱加入醋酸溶液OH-+CH3COOH═CH3COO-+H2O | |
| B. | 盐酸与小苏打溶液反应2H++CO32-═CO2↑+H2O | |
| C. | 氢氧化钡溶液中加入稀硫酸:Ba2++SO42-═BaSO4↓ | |
| D. | 金属钠与水反应Na+2H2O═Na++2OH-+H2↑ |
13.下列指定反应的离子方程式正确的是( )
| A. | 用氨水吸收足量的SO2:0H-+S02═HS03- | |
| B. | 氢氧化钡溶液与硫酸氢钠溶液反应至恰好呈中性:Ba2++2H++SO42-+20H-═BaS04↓+2H20 | |
| C. | 在加热条件下浓盐酸与Mn02反应制取少量氯气:Mn02+2H++2Cl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H20 | |
| D. | 向一定量的FeBr2溶液中通入过量Cl2:2Fe2++Cl2═2Fe3++2Cl- |
7.在某温度时,将n mol•L-1氨水滴入10mL 1.0mol•L-1盐酸中,溶液pH和温度随加入氨水体积变化曲线如图所示,下列有关说法正确的是( )

| A. | a点Kw=1.0×10-14 mol2•L-2 | |
| B. | 水的电离程度:b>c>a>d | |
| C. | b点:C(NH4+)>C(Cl-)>C(H+)>C(OH-) | |
| D. | 25℃时NH4Cl水解常数为(n-1)×10-7 mol•L-1(用n表示) |
8.化学是以实验为基础的自然科学,化学实验设计和操作中必须十分重视师生安全问题和环境保护问题.下列实验问题处理方法正确的是( )
| A. | 制氧气时排水法收集氧气后出现倒吸现象,应立即停止加热 | |
| B. | 在气体发生装置上直接点燃乙炔气体时,不需先检验乙炔气体的纯度 | |
| C. | 白磷在空气中易自燃,用剩的白磷可溶解于CS2后倒入垃圾箱 | |
| D. | 给试管中的液体加热时,可加入碎瓷片或不时移动试管,以免暴沸伤人 |