题目内容
13.下列指定反应的离子方程式正确的是( )| A. | 用氨水吸收足量的SO2:0H-+S02═HS03- | |
| B. | 氢氧化钡溶液与硫酸氢钠溶液反应至恰好呈中性:Ba2++2H++SO42-+20H-═BaS04↓+2H20 | |
| C. | 在加热条件下浓盐酸与Mn02反应制取少量氯气:Mn02+2H++2Cl$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H20 | |
| D. | 向一定量的FeBr2溶液中通入过量Cl2:2Fe2++Cl2═2Fe3++2Cl- |
分析 A.一水合氨在离子反应中保留化学式;
B.反应至恰好呈中性,反应生成硫酸钡、硫酸钠和水;
C.电荷、原子不守恒;
D.通入过量Cl2,亚铁离子、溴离子均被氧化.
解答 解:A.用氨水吸收足量的SO2的离子反应为NH3.H2O+S02═NH4++HS03-,故A错误;
B.氢氧化钡溶液与硫酸氢钠溶液反应至恰好呈中性的离子反应为Ba2++2H++SO42-+20H-═BaS04↓+2H20,故B正确;
C.在加热条件下浓盐酸与Mn02反应制取少量氯气的离子反应为Mn02+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H20,故C错误;
D.向一定量的FeBr2溶液中通入过量Cl2的离子反应为4Br-+2Fe2++3Cl2═2Br2+2Fe3++6Cl-,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的离子反应考查,综合性较强,题目难度不大,注意离子反应中保留化学式的物质.

练习册系列答案
相关题目
3.下列叙述正确的是( )
| A. | 乙烯和苯都能使酸性高锰酸钾溶液褪色 | |
| B. | 工业上用电解氯化镁溶液的方法生产金属镁 | |
| C. | 石油液化气、汽油和石蜡的主要成分都是碳氢化合物 | |
| D. | 淀粉和纤维素的分子式均为 (C6H10O5)n,它们互为同分异构体 |
1.可逆反应2NO2?2NO+O2在恒容密闭容器中进行,下列情况达到平衡状态的是( )
①单位时间内生成nmolO2的同时生成2nmolNO2
②混合气体的平均相对分子质量不再改变
③NO2、NO、O2的反应速率之比为2:2:1
④混合气体的颜色不再改变
⑤混合气体的密度不再改变.
①单位时间内生成nmolO2的同时生成2nmolNO2
②混合气体的平均相对分子质量不再改变
③NO2、NO、O2的反应速率之比为2:2:1
④混合气体的颜色不再改变
⑤混合气体的密度不再改变.
| A. | ①②④ | B. | ②③⑤ | C. | ①②⑤ | D. | ②④⑤ |
8.现有如图4个装置图,则以下说法中正确的是( )
| A. | 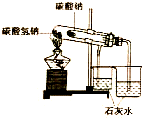 装置可用于比较NaHCO3和Na2CO3的稳定性 | |
| B. | 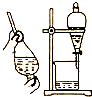 用酒精萃取溴水中的溴可选择装置 | |
| C. |  如图装置进行实验可看到酸性KMnO4溶液褪色 | |
| D. | 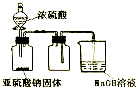 如图装置可用于实验室制取并收集少量SO2 |
18.下列实验操作中错误的是( )
| A. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| B. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| C. | 滴定时,左手控制滴定管活塞,右手握持锥形瓶,边滴边振荡,眼睛注视滴定管中的液面 | |
| D. | 称量时,称量放在称量瓶中,置于托盘天平的左盘,砝码放在托盘的天平的右盘中 |
2.已知:
2H2(g)+O2(g)=2H2O(l)△H=-572kJ•mol-1
H2(g)+0.5O2(g)=H2O(g)△H=-242kJ•mol-1
现有1mol液态水,蒸发时吸收的热量是( )
2H2(g)+O2(g)=2H2O(l)△H=-572kJ•mol-1
H2(g)+0.5O2(g)=H2O(g)△H=-242kJ•mol-1
现有1mol液态水,蒸发时吸收的热量是( )
| A. | 2.44 kJ | B. | 44 kJ | C. | 88 kJ | D. | 330 kJ |
19.下列解释事实的化学方程式或离子方程式,不正确的是( )
| A. | 在海带灰的浸出液(含有I-)中滴加H2O2得到I2:2I-+H2O2+2H+=I2+O2↑+2H2O | |
| B. | 自然界中正常的雨水呈酸性:H2O+CO2?H2CO3?H++HCO3- | |
| C. | 将1mol/L NaAlO2溶液和1mol/L的H2SO4溶液等体积均匀混合:3AlO2-+6H+=2Al(OH)3↓+Al3+ | |
| D. | 向明矾溶液中滴加氢氧化钡溶液至SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O |
20.氯水中存在多种分子和离子,可通过实验的方法加以确定.下列有关氯水中存在的粒子的说法错误的是( )
| A. | 加入含有 NaHSO4的石蕊试液,红色褪去,说明有Cl2分子存在 | |
| B. | 加入有色布条后,有色布条褪色,说明有 HCIO 分子存在 | |
| C. | 氯水呈浅黄绿色,且有刺激性气味,说明有Cl2分子存在 | |
| D. | 加入硝酸酸化的AgNO3溶液产生白色沉淀,说明有 Cl-存在 |
 .
.