题目内容
【题目】在CF3COOH水溶液中将甲烷直接转化为CF3COOCH3(水解生成CH3OH)的反应机理如图,下列说法正确的是
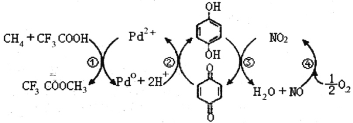
A.所含部分元素第一电离能:C<N<O<F
B.反应③的氧化剂为对苯二酚
C.上述反应的总反应式为:CH4+CF3COOH+![]() O2
O2 CF3COOCH3+H2O
CF3COOCH3+H2O
D.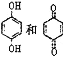 均可以与浓溴水反应,且反应类型相同
均可以与浓溴水反应,且反应类型相同
【答案】C
【解析】
A.同周期元素从左到右第一电离能呈增大趋势,第ⅤA元素原子最外层呈现半充满状态,第一电离能大于相邻元素,故应为C< O< N<F,A错误;
B.反应③中,N元素化合价降低,被还原,氧化剂为NO2,B错误;
C.根据图示可知,Pb2+等作催化剂,反应总方程式为:CH4+CF3COOH+![]() O2
O2 CF3COOCH3+H2O,C正确;
CF3COOCH3+H2O,C正确;
D.![]() 含有酚羟基,可与浓溴水发生取代反应;
含有酚羟基,可与浓溴水发生取代反应;![]() 含有碳碳双键,与溴水发生加成反应,反应类型不同,D错误;
含有碳碳双键,与溴水发生加成反应,反应类型不同,D错误;
答案选C。

 名校课堂系列答案
名校课堂系列答案【题目】甲醇与水蒸气重整制氢可直接用于燃料电池。回答下列问题:
(1)已知:甲醇分解反应:CH3OH(g)![]() CO(g)+2H2(g) △H1=________ kJ·mol-1水蒸气变换反应:CO(g)+H2O(g)
CO(g)+2H2(g) △H1=________ kJ·mol-1水蒸气变换反应:CO(g)+H2O(g)![]() CO2(g)+H2(g) △H2=-41.20 kJ·mol-1,则CH3OH(g)+H2O(g)
CO2(g)+H2(g) △H2=-41.20 kJ·mol-1,则CH3OH(g)+H2O(g)![]() CO2(g)+3H2(g)△H3=+49.44kJ·mol-1。
CO2(g)+3H2(g)△H3=+49.44kJ·mol-1。
(2)科学家通过密度泛函理论研究甲醇与水蒸气重整制氢反应机理时,得到甲醇在Pd(Ⅲ)表面发生解离时四个路径与相对能量关系如图所示,其中附在Pd(Ⅲ)表面的物种用*标注。此历程中活化能最小的反应方程式为_________________________。
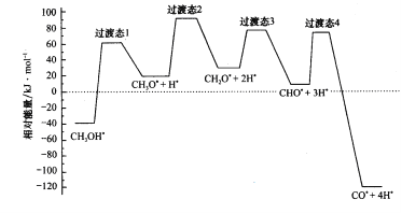
(3)在0.1MPa下,将总进料量1 mol且n(CH3OH):n(H2O)=1:1.3的混合气体充入一刚性密闭容器中反应。
①实验测得水煤气变换反应的速率随温度的升高明显下降,原因是__________。
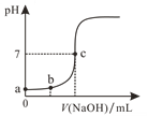
②平衡时,测得CH3OH的含量在给定温度范围内极小,H2、H2O(g)、CO、CO2四种组分含量与反应温度关系如图所示,试解释a的含量约是c的含量3倍的原因__________。

(4)297 K时,向密闭容器Ⅰ(体积为4L)和Ⅱ(体积为8L)中分别充入下列物质发生反应,
编号 | CO(mol) | H2(mol) | CH3OH(mol) |
Ⅰ | 4 | a | 0 |
Ⅱ | 4 | 4 | 4 |
达平衡时两个容器中c(H2)相等且c(H2)=0.5mol/L。则
①a=_____________。
②该温度时,Ⅰ中反应的K=___________。
③Ⅱ中按表格数据充入反应物此时反应的方向__________(填“正向进行”、“平衡”或“逆向进行”)。