题目内容
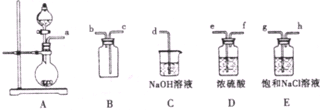
如图是实验室制取纯净、干燥的氯气的实验装置图.请回答下列问题:

(1)烧瓶中产生氯气中可能含有杂质气体 .
(2)该实验装置中还缺少的仪器是 .
(3)丁装置的作用是 ,离子方程式是 .
(4)为除去氯气中杂质,洗气瓶甲装有 ,乙装有 .

(1)烧瓶中产生氯气中可能含有杂质气体
(2)该实验装置中还缺少的仪器是
(3)丁装置的作用是
(4)为除去氯气中杂质,洗气瓶甲装有
考点:氯气的实验室制法
专题:卤族元素
分析:(1)氯化氢具有挥发性,所以制取的氯气中会混有氯化氢气体;
(2)根据反应原理MnO2+4HCl (浓)
MnCl2+Cl2↑+2H2O判断反应条件及缺少的仪器;
(3)氯气有毒不能排放到空气中,需要用氢氧化钠溶液吸收;
生成的氯气中含有氯化氢和水蒸气,通过装置②吸收氯化氢,通过装置③吸收水蒸气,选择浓硫酸;
(4)生成的氯气中含有氯化氢和水蒸气,通过装置甲吸收氯化氢,通过装置乙吸收水蒸气,选择浓硫酸.
(2)根据反应原理MnO2+4HCl (浓)
| ||
(3)氯气有毒不能排放到空气中,需要用氢氧化钠溶液吸收;
生成的氯气中含有氯化氢和水蒸气,通过装置②吸收氯化氢,通过装置③吸收水蒸气,选择浓硫酸;
(4)生成的氯气中含有氯化氢和水蒸气,通过装置甲吸收氯化氢,通过装置乙吸收水蒸气,选择浓硫酸.
解答:
解:(1)实验室制取氯气利用二氧化锰和浓盐酸加热反应生成,反应的化学方程式为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,氯化氢具有挥发性,所以制取的氯气中会混有装杂质HCl,
故答案为:HCl;
(2)实验室制取氯气的方程式为:MnO2+4HCl (浓)
MnCl2+Cl2↑+2H2O,该反应需要加热才能进行,所以需要使用酒精灯和石棉网,装置中缺少的仪器为酒精灯、石棉网,
故答案为:酒精灯、石棉网;
(3)氯气有毒不能排放到空气中,需要用氢氧化钠溶液吸收,装置丁的作用是吸收多余的氯气,反应的离子方程式为:Cl2+2OH?=Cl?+ClO?+H2O,
故答案为:吸收多余的氯气;Cl2+2OH?=Cl?+ClO?+H2O;
(4)生成的氯气中含有氯化氢和水蒸气,通过装置甲中饱和食盐水可以吸收氯化氢,通过装置乙中浓硫酸吸收水蒸气,
故答案为:饱和食盐水;浓硫酸.
| ||
故答案为:HCl;
(2)实验室制取氯气的方程式为:MnO2+4HCl (浓)
| ||
故答案为:酒精灯、石棉网;
(3)氯气有毒不能排放到空气中,需要用氢氧化钠溶液吸收,装置丁的作用是吸收多余的氯气,反应的离子方程式为:Cl2+2OH?=Cl?+ClO?+H2O,
故答案为:吸收多余的氯气;Cl2+2OH?=Cl?+ClO?+H2O;
(4)生成的氯气中含有氯化氢和水蒸气,通过装置甲中饱和食盐水可以吸收氯化氢,通过装置乙中浓硫酸吸收水蒸气,
故答案为:饱和食盐水;浓硫酸.
点评:本题考查了氯气的实验室制法,题目难度不大,注意氯气的实验室制法以及氯气与次氯酸的性质的不同,明确饱和食盐水、浓硫酸的作用及尾气处理方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列物质分类的正确组合是( )
| 混合物 | 碱 | 盐 | 碱性氧化物 | 酸性氧化物 | |
| A | 液态氯气 | 苛性钠 | 硫酸铜 | 氧化铁 | 二氧化碳 |
| B | 氯水 | 烧碱 | 食盐 | 氧化钠 | 氧化铝 |
| C | 84消毒液 | 纯碱 | 石灰石 | 氨气 | 水 |
| D | 漂白粉 | 熟石灰 | 苏打 | 生石灰 | 二氧化硫 |
| A、A | B、B | C、C | D、D |
新能源的开发利用是人类社会可持续发展的重要课题.下列属于新能源的是( )
| A、太阳能 | B、煤炭 |
| C、天然气 | D、石油 |
下列关于电解质溶液的叙述正确的是( )
| A、常温下,将pH均为12的氨水和NaOH溶液分别加水稀释100倍后,NaOH溶液的pH较大 |
| B、将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低 |
| C、一元酸与一元碱恰好完全反应后的溶液中一定存在c(H+)=c(OH-) |
| D、pH=2和pH=1的硝酸中c(H+)之比为1:10 |