题目内容
8.某同学猜测,铝热反应所得到的熔融物是铁铝合金.(1)根据已有知识找出一种验证产物中有Fe的最简单方法用磁铁吸引,如果能吸引,说明有铁生成
(2)设计一个简单的实验方案,证明上述所得的熔融物中含有金属铝.(只用反应离子方程式表示)2Al+2OH-+2H2O=2AlO2-+3H2↑.
(3)工业上冶炼单质铝的反应方程式是2Al2O3(熔融)$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑.
分析 (1)Fe能被磁铁吸引,据此可鉴别产物中是否有Fe;
(2)Al能溶于NaOH溶液且生成氢气;
(3)工业冶炼铝是利用惰性电极电极熔融氧化铝得到.
解答 解:(1)Fe能被磁铁吸引,所以最简单的办法是用磁铁吸引,如果能吸引,说明有铁生成,
故答案为:用磁铁吸引,如果能吸引,说明有铁生成;
(2)Fe、Al、Fe2O3、Al2O3中只有Al能溶于NaOH溶液且生成氢气,向溶液中加入NaOH溶液,根据固体是否溶解且生成氢气判断是否含有Al,离子方程式为2Al+2OH-+2H2O=2AlO2-+3H2↑,
故答案为:2Al+2OH-+2H2O=2AlO2-+3H2↑;
(3)工业冶炼铝是利用惰性电极电极熔融氧化铝得到,阳极是氯离子失电子生成氯气,阴极是铝离子得到电子生成铝,反应的化学方程式为:2Al2O3(熔融)$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑;
故答案为:2Al2O3(熔融)$\frac{\underline{\;通电\;}}{\;}$4Al+3O2↑.
点评 本题考查了铝热反应产物的检验,题目难度中等,涉及铁的性质及检验、工业冶炼铝的方法、离子方程式书写等知识,试题侧重考查学生的分析、理解能力及灵活应用能力.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
19.下列物质中,与水反应剧烈程度最强的是( )
| A. | Li | B. | Na | C. | K | D. | Cs |
16.下表给出了六种元素的相关信息,其中A、B、C、D、E为短周期元素.
请根据以上信息回答问题:
(1)A元素符号H F元素的名称铁
(2)C元素在周期表中的位置第2周期VA族
(3)D元素原子结构示意图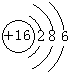
(4)E元素最高价氧化物对应水化物化学式为NaOH
(5)有A、B和E三种元素组成的化合物属于离子晶体(填“原子”、“离子”或“分子”),其晶体中含有的化学键类型为离子键、共价键.
(6)B和D对应的气态氢化物中,热稳定性较强的是H2O,熔沸点较高的是H2O.(用具体的化学式表示)
(7)D的最高价含氧酸稀溶液与F单质反应的离子方程式Fe+2H+=Fe2++H2↑.
| 元素 | 相 关 信 息 |
| A | 在常温、常压下,其单质是气体,随着人类对环境的认识和要求的提高,它将成为倍受青睐的清洁燃料. |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障. |
| C | 植物生长三种必需元素之一,它能形成多种氧化物,其氢化物是中学化学里学习的唯一的碱性气体,能使湿润的红色石蕊试纸变蓝. |
| D | 室温下其单质呈淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰. |
| E | 它在空气剧烈燃烧,有黄色火焰,生成的淡黄色固态化合物可用于潜水艇的供氧剂. |
| F | 它是人体不可缺少的微量元素,其单质也是应用最广的金属原材料,常用于制造桥梁、轨道等. |
(1)A元素符号H F元素的名称铁
(2)C元素在周期表中的位置第2周期VA族
(3)D元素原子结构示意图

(4)E元素最高价氧化物对应水化物化学式为NaOH
(5)有A、B和E三种元素组成的化合物属于离子晶体(填“原子”、“离子”或“分子”),其晶体中含有的化学键类型为离子键、共价键.
(6)B和D对应的气态氢化物中,热稳定性较强的是H2O,熔沸点较高的是H2O.(用具体的化学式表示)
(7)D的最高价含氧酸稀溶液与F单质反应的离子方程式Fe+2H+=Fe2++H2↑.
3.实验室需要取用l2.20mL0.1000mol/L的盐酸,计量容器应该是( )
| A. | 量筒 | B. | 碱式滴定管 | C. | 酸式滴定管 | D. | 容量瓶 |
13.下列说法正确的是(NA为阿伏加德罗常数)( )
| A. | 124 g P4含有P-P键的个数为4NA | |
| B. | 12 g石墨中含有C-C键的个数为1.5NA | |
| C. | 12 g金刚石中含有C-C键的个数为4NA | |
| D. | SiO2晶体中存在四面体结构单元,O处于中心,Si处于4个顶角 |
20.只用一种试剂就能区别FeCl3和FeCl2二种溶液,该试剂可用( )
①硫氰化钾溶液 ②NaOH溶液 ③氯水 ④铁粉.
①硫氰化钾溶液 ②NaOH溶液 ③氯水 ④铁粉.
| A. | ①② | B. | ①③ | C. | ②③ | D. | ②④ |
17.2008年8月25日,十一届全国人大常委会第四次会议正式对《食品安全法(草案)》进行了二审,表明国家对食品安全问题越来越重视.工商人士提醒消费者,长期食用二氧化硫含量超标的食品不仅会破坏维生素B1,还会影响人体对钙的吸收.下列说法中一定错误 的是( )
| A. | 二氧化硫遇水生成亚硫酸,容易引起胃肠道反应 | |
| B. | 人体直接吸入二氧化硫易引起呼吸道疾病 | |
| C. | 二氧化硫引起的环境问题主要是酸雨 | |
| D. | 可通过服入碱性物质(如NaOH)的方法来消除二氧化硫中毒 |