题目内容
【题目】反应A(g)+B(g)===C(g) ΔH,分两步进行:
①A(g)+B(g)===X(g) ΔH1
②X(g)===C(g) ΔH2
反应过程中能量变化如下图所示,E1表示A+B===X的活化能,下列说法正确的是
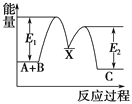
A. ΔH1=ΔH-ΔH2>0
B. X是反应A(g)+B(g)===C(g)的催化剂
C. E2是反应②的反应热
D. ΔH=E1-E2
【答案】A
【解析】A、①+②得出A(g)+B(g)→C(g) △H=△H1+△H2,反应物的总能量高于生成物的总能量,此反应是放热反应,△H1=△H-△H2,依据信息,反应物能量低于X的能量,此反应属于吸热反应,△H1=△H-△H2>0,选项A正确;B、从图中看出,X应为反应的中间产物,不是催化剂,选项B错误;C、E2应为反应②的逆反应的活化能,不是其反应热,选项C错误;D、△H是反应物和生成物总能量的差值,未给出反应①的逆反应的活化能和反应②的活化能,无法计算ΔH,选项D错误。答案选A。

练习册系列答案
 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案
相关题目