题目内容
5.已知X、Y、Z均为短周期元素,且原子序数依次递增,其中X元素的单质是自然界最轻的气体,Y元素原子的最外层电子数是次外层电子数的2倍,Z元素的氧化物ZO2是形成酸雨的主要气体.(1)写出X的元素符号H;
(2)画出Y的原子结构示意图
 ;
;(3)Y元素在元素周期表中的位置是第二周期第IVA族;
(4)Y与Z两种元素的最高价氧化物对应水化物的酸性较强的是H2SO4 (填分子式).
分析 X、Y、Z均为短周期元素,且原子序数依次递增,其中X元素的单质是自然界最轻的气体,该气体为氢气,则X为H元素;Y元素原子的最外层电子数是次外层电子数的2倍,Y有2个电子层,最外层电子数为4,故Y为C元素;Z元素的氧化物ZO2是形成酸雨的主要气体,该气体为二氧化硫,则Z为S元素,据此进行解答.
解答 解:X、Y、Z均为短周期元素,且原子序数依次递增,其中X元素的单质是自然界最轻的气体,故X为H元素;Y元素原子的最外层电子数是次外层电子数的2倍,Y有2个电子层,最外层电子数为4,故Y为C元素;Z元素的氧化物ZO2是形成酸雨的主要气体,Z为S元素,
(1)由上述分析可知,X为H元素,故答案为:H;
(2)Y为C元素,碳原子核外有6个电子,有2个电子层,最外层电子数为4,原子结构示意图为: ,故答案为:
,故答案为: ;
;
(3)Y为C元素,原子质子数为6,有2个电子层,最外层电子数为4,在元素周期表中处于第二周期第IVA族,故答案为:第二周期第IVA族;
(4)非金属性越强,最高价氧化物对应水化物的酸性越强,非金属性S>C,所以两种元素的最高价氧化物对应水化物的酸性较强的为H2SO4,故答案为:H2SO4.
点评 本题考查位置、结构与性质关系的应用,题目难度中等,推断各元素为解答关键,注意掌握元素周期表结构、元素周期律内容,试题侧重考查学生的分析、理解能力及灵活应用能力.

练习册系列答案
相关题目
15.钡盐行业生产中排出大量的钡泥 主要含有【BaCO3、BaSiO3、BaSO3、Ba(FeO2)2】等.某主要生产BaCl2、BaCO3、BaSO4的化工厂利用钡泥制取Ba(NO3)2,其部分工艺流程如下
已知部分离子沉淀所需的pH如下表
问答下列问题
(1)上述③过滤操作中除要用到玻璃棒,铁架台,烧杯等还缺的玻璃仪器有漏斗,废渣中的主要化学物质是BaSiO3、H2SiO3、Fe(OH)3、BaSO4(写化学式)
(2)写出酸溶过程中涉及氧化还原反应的离子方程式3BaSO3+2H++2NO3-=3BaSO4+2NO↑+H2O
(3)该厂结合本厂实际,选用的X为BaCO3(填化学式);中和Ⅰ使溶液中Fe3+、H+(填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)
(4)上述④洗涤的目的是减少废渣中可溶性钡盐对环境的污染.
(5)由于废渣给周围环境造成了一定的污染,该工厂想设计一个方案,将工厂废渣进行分离,并制备生产光导纤维的主要原材料,请你按示例简要设计实验分案(示例:取物质A$\stackrel{加热}{→}$$\stackrel{蒸发}{→}$ 得到物质B)
废渣$\stackrel{适量氢氧化钾}{→}$$\stackrel{搅拌过滤}{→}$滤液$\stackrel{加入足量盐酸}{→}$$\stackrel{搅拌过滤}{→}$$\stackrel{加热}{→}$二氧化硅.

已知部分离子沉淀所需的pH如下表
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.7 | 7.5 | 1.4 |
| 沉淀完全pH | 6.7 | 14 | 3.7 |
(1)上述③过滤操作中除要用到玻璃棒,铁架台,烧杯等还缺的玻璃仪器有漏斗,废渣中的主要化学物质是BaSiO3、H2SiO3、Fe(OH)3、BaSO4(写化学式)
(2)写出酸溶过程中涉及氧化还原反应的离子方程式3BaSO3+2H++2NO3-=3BaSO4+2NO↑+H2O
(3)该厂结合本厂实际,选用的X为BaCO3(填化学式);中和Ⅰ使溶液中Fe3+、H+(填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)
(4)上述④洗涤的目的是减少废渣中可溶性钡盐对环境的污染.
(5)由于废渣给周围环境造成了一定的污染,该工厂想设计一个方案,将工厂废渣进行分离,并制备生产光导纤维的主要原材料,请你按示例简要设计实验分案(示例:取物质A$\stackrel{加热}{→}$$\stackrel{蒸发}{→}$ 得到物质B)
废渣$\stackrel{适量氢氧化钾}{→}$$\stackrel{搅拌过滤}{→}$滤液$\stackrel{加入足量盐酸}{→}$$\stackrel{搅拌过滤}{→}$$\stackrel{加热}{→}$二氧化硅.
16.1mol某烃在氧气中充分燃烧,需要消耗氧气179.2L(标准状况下).它在光照的条件下与氯气反应能生成三种不同的一氯取代物.该烃的结构简式是( )
| A. | CH3CH2CH2CH2CH3 | B. |  | C. | 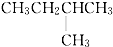 | D. | 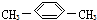 |
20. 同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )
同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )
 同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )
同一短周期内主族元素最高价氧化物对应水化物相同浓度稀溶液的pH与原子半径的关系如图,下列说法正确的是( )| A. | 原子序数:W>Z>X | |
| B. | 气态氢化物的稳定性:N>R | |
| C. | Y和W形成共价化合物 | |
| D. | X和Z两者最高价氧化物对应的水化物能相互反应 |
10.已知: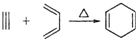 ,如果要合成
,如果要合成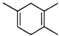 所用的原始原料可以是( )
所用的原始原料可以是( )
 ,如果要合成
,如果要合成 所用的原始原料可以是( )
所用的原始原料可以是( )| A. | 2-甲基-l,3-丁二烯 和 2-丁炔 | B. | 1,3-戊二烯 和 2-丁炔 | ||
| C. | 2,3-二甲基-1,3-戊二烯 和 乙炔 | D. | 2,3-二甲基-l,3-丁二烯 和 丙炔 |
17.一氧化碳、烯烃和氢气在催化剂作用下发生烯烃的醛化反应,又叫羰基的合成.由乙烯可制丙醛:
CH2=CH2+CO+H2$\stackrel{催化剂}{→}$CH3CH2CHO.由分子式为C4H8的烯烃进行醛化反应得到的醛,共有几种?( )
CH2=CH2+CO+H2$\stackrel{催化剂}{→}$CH3CH2CHO.由分子式为C4H8的烯烃进行醛化反应得到的醛,共有几种?( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
15.与Ne的核外电子排布相同的离子跟与Ar的核外电子排布相同的离子所形成的化合物是( )
| A. | Na2S | B. | CCl4 | C. | KCl | D. | Na2O |