题目内容
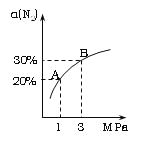
【题目】常温下,向1L0.1mol·L-1一元酸HR溶液中逐渐通入氨气[已知常温下NH3·H2O电离平衡常数K=1.76×10-5],使溶液温度和体积保持不变,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是

A.0.1mol·L-1HR溶液的pH为5
B.当pH=6时,水电离出的氢离子浓度为1.0×10-6
C.当通入0.1 mol NH3时,c(![]() )>c(R-)>c(H+)>c(OH-)
)>c(R-)>c(H+)>c(OH-)
D.当 pH=7时,c(![]() )=c(R-)
)=c(R-)
【答案】D
【解析】
A.据图可知lg![]() =0时,溶液pH=5,lg
=0时,溶液pH=5,lg![]() =0,则
=0,则![]() =1,所以此时Ka=
=1,所以此时Ka=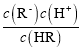 =c(H+) =10-5;设0.1mol·L-1HR溶液中c(H+) =a,则有
=c(H+) =10-5;设0.1mol·L-1HR溶液中c(H+) =a,则有![]() ,解得a约为10-3mol/L,所以溶液pH为3,故A错误;
,解得a约为10-3mol/L,所以溶液pH为3,故A错误;
B.pH等于6时溶液中的溶质为NH4R和HR,此时水的电离受到抑制,溶液中的c(H+) =10-6 mol/L,但不是全部由水电离,溶液中c(OHˉ) =10-8 mol/L,且全部由水电离,而水电离出的氢离子和氢氧根相等,所以水电离出的氢离子浓度约为10-8 mol/L,故B错误;
C.1L0.1mol·L-1HR溶液中n(HR)=0.1mol,所以当通入0.1 mol NH3时,溶液中的溶质为NH4R,Rˉ水解使溶液显碱性,铵根水解使溶液显酸性,根据题意可知常温下NH3·H2O电离平衡常数K=1.76×10-5> Ka(HR),一水合氨的电离程度更大,所以Rˉ的水解程度更大,所以溶液显碱性,则c(OH-)>c(H+),故C错误;
D.当 pH=7时,溶液中c(OH-)=c(H+),结合电荷守恒:c(H+)+c(![]() )=c(R-)+ c(OH-)可知c(
)=c(R-)+ c(OH-)可知c(![]() )=c(R-),故D正确;
)=c(R-),故D正确;
故答案为D。

 轻巧夺冠周测月考直通中考系列答案
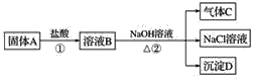
轻巧夺冠周测月考直通中考系列答案【题目】FeCl2是一种常用的还原剂、媒染剂。某化学实验小组在实验室里用如下两种方法来制备无水FeCl2。有关物质的性质如下:
C6H5Cl(氯苯) | C6H4Cl2(二氯苯) | FeCl3 | FeCl2 | |
溶解性 | 不溶于水,易溶于苯、乙醇 | 不溶于C6H5Cl、C6H4Cl2、苯,易溶于乙醇,易吸水 | ||
熔点/℃ | -45 | 53 | 304 | 670 |
沸点/℃ | 132 | 173 | 316,易升华 | 700 |
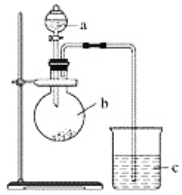
(1)用H2还原无水FeCl3制取FeCl2。有关装置如下:

①H2还原少量无水FeCl3制取FeCl2的化学方程式为_____________。
②按气流由左到右的方向,上述仪器的连接顺序为B→A→___→___→___→E(填字母,装置可多次使用);A中长颈漏斗的作用_____________。
③C中盛放的试剂是_____________。
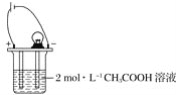
(2)利用反应2FeCl3+C6H5Cl![]() 2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按如图装置,在三颈烧瓶中放入32.5 g无水氯化铁和过量的氯苯,反应开始前先通N2一段时间,控制反应温度在一定范围加热3 h,反应完成后继续通一段时间N2至装置冷却后,分离提纯得到粗产品。
2FeCl2+C6H4Cl2+HCl↑,制取无水FeCl2并测定FeCl3的转化率。按如图装置,在三颈烧瓶中放入32.5 g无水氯化铁和过量的氯苯,反应开始前先通N2一段时间,控制反应温度在一定范围加热3 h,反应完成后继续通一段时间N2至装置冷却后,分离提纯得到粗产品。

①仪器a的作用是__________。
②反应中提供过量氯苯的作用是__________。
③反应结束后,冷却实验装置A,将三颈烧瓶内物质倒出,经过滤、洗涤、干燥后,得到粗产品。洗涤所用的试剂可以是____,回收滤液中C6H5Cl的操作方法是______。
④反应后将锥形瓶中溶液配成250 mL,量取25.00 mL所配溶液,用0.400 mol/L的NaOH溶液滴定,终点时消耗NaOH溶液为19.60 mL,则氯化铁的转化率为__________。