题目内容
10.下列物质中的杂质(括号内为杂质)不能用加热法直接除去的是( )| A. | Fe粉(硫粉) | B. | Na2CO3粉末(NaHCO3) | ||
| C. | NaCl(碘) | D. | KMnO4(MnO2) |
分析 原物质与杂质发生化学反应时不能利用加热法除杂,若两种物质中杂质加热分解或升华可除杂,以此来解答.
解答 解:A.加热时Fe与S反应生成FeS,不能加热除杂,可利用磁铁分离,故A选;
B.加热时碳酸氢钠分解生成碳酸钠,可加热除杂,故B不选;
C.加热时碘升华,与NaCl分离,可加热除杂,故C不选;
D.加热时高锰酸钾分解,不能加热除杂,应溶解、过滤、蒸发分离,故D选;
故选AD.
点评 本题考查混合物的分离提纯,为高频考点,把握物质的性质、性质差异、发生的反应等为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
1.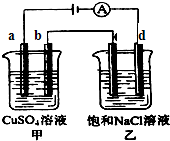 如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
 如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )
如图两个电解槽中,a、b、c、d均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中正确的是( )| A. | 甲烧杯中a极上最多可析出铜0.64g | |
| B. | 甲烧杯中b极上电极反应式4OH--4e-═2H2O+O2↑ | |
| C. | 乙烧杯中滴入酚酞试液,d极附近先变红 | |
| D. | 烧杯中c极上电极反应式为4H++4e-═2H2↑ |
5.常温下用pH为3的某酸溶液分别与pH都为11的氨水、氢氧化钠溶液等体积混合得到a、b两种溶液,关于这两种溶液酸碱性的描述正确的是( )
①b不能显碱性 ②a可能显酸性或碱性 ③a不可能显酸性 ④b可能显碱性或酸性.
①b不能显碱性 ②a可能显酸性或碱性 ③a不可能显酸性 ④b可能显碱性或酸性.
| A. | ①② | B. | ③④ | C. | ①③ | D. | ②④ |
15.下列有关酸、碱、盐的说法中,错误的是( )
| A. | 酸根中可能含有氧元素 | B. | 正盐中一定不含氢元素 | ||
| C. | 碱中一定含有氢元素和氧元素 | D. | 酸式盐中含有氢元素 |
2.下列有关试剂的保存方法正确的是( )
①NaOH固体保存在配有橡皮塞的细口瓶中;
②Na2CO3溶液通常保存在配有橡皮塞的细口瓶中;
③液溴通常用水封保存;
④锂保存在煤油中;
⑤浓硝酸通常保存在棕色细口瓶中.
①NaOH固体保存在配有橡皮塞的细口瓶中;
②Na2CO3溶液通常保存在配有橡皮塞的细口瓶中;
③液溴通常用水封保存;
④锂保存在煤油中;
⑤浓硝酸通常保存在棕色细口瓶中.
| A. | ①③⑤ | B. | ②③⑤ | C. | ②④⑤ | D. | ①③④ |
19.某一元醛发生银镜反应,生成金属银4.32g,等量该醛完全燃烧后,可生成水1.08g,则此醛可以是下列中的( )
| A. | 丙醛(CH3CH2CHO) | B. | 丙烯醛(CH2=CH-CHO) | ||
| C. | 丁醛(C3H7CHO) | D. | 丁烯醛(CH3-CH=CH-CHO) |
20.下列反应的离子方程式书写正确的是( )
| A. | 向NaOH溶液中通入少量CO2:OH-+CO2═HCO3- | |
| B. | 用氨水吸收少量SO2:2NH3•H2O+SO2═2NH4++SO32-+H2O | |
| C. | Al(NO3)2溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+2H2O+4NH4+ | |
| D. | 向Fe2(SO4)3的酸性溶液中通入足量H2S:Fe3++H2S═Fe2++S↓+2H+ |
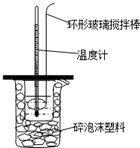 用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L的盐酸与50mL0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: