题目内容
13.按要求完成下列化学方程式或离子方程式.(l)过氧化钠用于呼吸面具中,发生反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2.
(2)与化合物反应中氯气只作氧化剂的化学方程式:2Fe+3Cl2$\frac{\underline{\;点燃\;}}{\;}$2FeCl3.
(3)金属阳离子作氧化剂的离子方程式:2Fe3++Cu═2Fe2++Cu2+.
分析 (1)过氧化钠和二氧化碳反应生成碳酸钠和氧气;
(2)氯气与金属单质的反应中,氯气只做氧化剂,如氯气与铁生成氯化铁的反应;
(3)铁离子与铜反应生成亚铁离子和铜的反应中,铁离子做氧化剂.
解答 解:(1)过氧化钠和二氧化碳反应生成碳酸钠和氧气,反应的化学方程式为:2Na2O2+2CO2═2Na2CO3+O2↑,
故答案为:2Na2O2+2CO2=2Na2CO3+O2;
(2)铁在氯气中燃烧生成氯化铁,反应的方程式为:2Fe+3Cl2 $\frac{\underline{\;点燃\;}}{\;}$2FeCl3,该反应中氯气只做氧化剂,
故答案为:2Fe+3Cl2 $\frac{\underline{\;点燃\;}}{\;}$2FeCl3;
(3)氯化铁和Cu反应生成氯化亚铁和氯化铜,离子反应为Cu+2Fe3+═2Fe2++Cu2+,
故答案为:2Fe3++Cu═2Fe2++Cu2+.
点评 本题考查了离子方程式、化学方程式的书写,题目难度中等,明确离子方程式、化学方程式是书写原则为解答关键,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.

练习册系列答案
相关题目
13.下列各项中表达正确的是( )
| A. | 氟原子的结构示意图: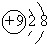 | B. | 乙烯结构式:CH2=CH2 | ||
| C. | 乙炔球棍模型: | D. | NH3的电子式: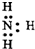 |
1.下列物质既能由金属和酸反应获得,也能通过金属和氯气反应获得的是( )
| A. | CuCl2 | B. | FeCl2 | C. | FeCl3 | D. | NaCl |
8.下列物质的分类中.正确的一组是( )
| 分类、选项 | 酸 | 碱 | 盐 | 碱性氧化物 |
| A | H2SO4 | Na2CO3 | NaHCO3 | CaO |
| B | HCl | NH3•H2O | NaCl | Na2O |
| C | CO2 | Cu(OH)2 | MgCl2 | Na2O |
| D | HNO3 | KOH | CaO | CO |
| A. | A | B. | B | C. | C | D. | D |
5.已知:2H2(g)+O2(g)═2H2O(l)△H=-571.6kJ•mol-1
2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1 452kJ•mol-1
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列说法正确的是( )
2CH3OH(l)+3O2(g)═2CO2(g)+4H2O(l)△H=-1 452kJ•mol-1
H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ•mol-1
下列说法正确的是( )
| A. | H2(g)的燃烧热为571.6 kJ•mol-1 | |
| B. | $\frac{1}{2}$H2SO4(aq)+$\frac{1}{2}$Ba(OH)2(aq)═$\frac{1}{2}$BaSO4(s)+H2O(l)△H=-57.3 kJ•mol-1 | |
| C. | 同质量的H2(g)和CH3OH(l)完全燃烧,H2(g)放出的热量多 | |
| D. | 3H2(g)+CO2(g)═CH3OH(l)+H2O(l)△H=+131.4 kJ•mol-1 |
2.下列物质属于非电解质的是( )
| A. | CO2 | B. | Cu | C. | NaCl | D. | CH3COOH |
3.下列事实不能用勒夏特列原理解释的是( )
| A. | 工业生产硫酸的过程中使用过量的氧气,以提高二氧化硫的转化率 | |
| B. | 合成氨工厂通常采用20MPa~50MPa压强,以提高原料的利用率 | |
| C. | 实验室用排饱和食盐水的方法收集氯气 | |
| D. | 用铁触媒作催化剂加快化学反应速率 |
 .
.