题目内容
4.等质量的O2和O3,其分子的物质的量比为3:2,原子数之比为1:1,标准状况下的体积之比为3:2.同温同压下,同体积的CH4和CO2的质量之比为4:11,密度之比为4:11.分析 O2和O3都是由氧原子构成,等质量相等说明氧原子的物质的量相等,所以O2和O3的分子的物质的量之比为3:2,标准状况下的体积之比等于物质的量之比,根据阿伏加德罗定律可知,同温同压下同体积的CH4和CO2的物质的量相同,根据$ρ=\frac{m}{V}$,体积相同密度之比等于质量之比.
解答 解:O2和O3都是由氧原子构成,等质量相等说明氧原子的物质的量相等,所以O2和O3的分子的物质的量之比为3:2,标准状况下的体积之比为3:2,根据阿伏加德罗定律可知,同温同压下同体积的CH4和CO2的物质的量相同,所以质量之比为16:44=4:11,密度之比为4:11,故答案为:3:2;1:1;3:2;4:11;4:11.
点评 本题考查阿伏加德罗定律及其推论,涉及物质的量的有关计算,题目难度不大,注意相关计算公式的运用.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
12.在一定条件下,等物质的量的乙烯和苯分别和足量氢气发生加成反应,消耗氢气的物质的量之比为( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 1:4 |
19.同温、同压下等质量的SO2气体和CO2气体,下列有关比较的叙述中不正确的是( )
| A. | 物质的量比为11:16 | B. | 密度比为16:11 | ||
| C. | 体积比为16:11 | D. | 体积比为11:16 |
9.下列物质间分子间作用力最大的是( )
| A. | I2 | B. | Br2 | C. | Cl2 | D. | F2 |
16.放射性核素12553I可用于治肿瘤,下列关于12553I的叙述正确的是( )
| A. | 12553I 原子核内中子数为53 | |
| B. | 12553I原子核外电子数为72 | |
| C. | 12553I 和12753I互为同位素 | |
| D. | 12553I代表有53个质子和125个中子的碘原子 |
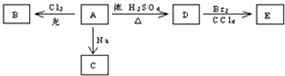 化合物A(C4H10O)是一种有机溶剂.A可以发生如图变化:
化合物A(C4H10O)是一种有机溶剂.A可以发生如图变化: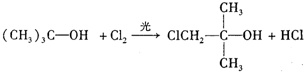 .
. .
.