题目内容
【题目】新春佳节少不了饮酒,土法酿造葡萄酒(只加糖的纯天然酿酒法)容易出问题,有报道说,喝了自制葡萄酒差点失明。主要原因是发酵过程产生的菌种多达百种,难以控制,而产生对神经有毒的甲醇等物质。科学酿酒须加SO2等辅料。我国国家标准(GB2760-2014)规定葡萄酒中SO2的残留量≤0.25g/L。
(1)葡萄酒中添加SO2的作用可能是________。
A.抗氧化 B. 氧化细菌 C.增酸作用 D. 漂白
I.实验方案一
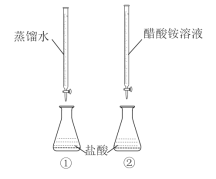
利用SO2的漂白性检测干白葡萄酒(液体为无色)中的SO2或H2SO3。设计如图的实验:
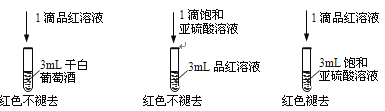
(2)甲同学得出实验结论: 干白葡萄酒中不含SO2或H2SO3。这个结论是否合理?说明理由___________。
Ⅱ.实验方案二
如图是在实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。
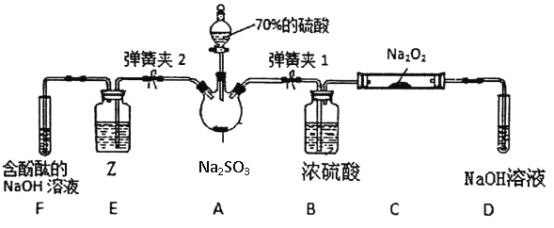
(3)关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没瓶中固体,写出A装置反应的化学方程式______,C中每消耗2molNa2O2,则转移电子数___________。
(4)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F中,为了证明SO2有还原性,并从绿色化学的角度考虑,则Z试剂可以是____,反应的离子反应方程式为____________,现象是_______。
【答案】AC 不合理;实验对比说明浓度低的亚硫酸不能使品红褪色,葡萄酒中的SO2含量很低,所以也不能使品红褪色 Na2SO3 +H2SO4 = Na2SO4 + SO2↑+ H2O 4NA 酸性KMnO4 2MnO4— + 5SO2 +2 H2O = 2Mn2+ + 5SO42— + 4H+(或FeCl3溶液,SO2 +2 Fe3+ +2 H2O = 2 Fe 2+ + SO42— + 4H+) 红色溶液变浅或褪色(或溶液由棕黄色变为浅绿色)
【解析】
(1)二氧化硫具有较强的还原性,可以防止葡萄酒被氧化,二氧化硫的水溶液显酸性,可以增强葡萄酒的酸性,二氧化硫有漂白性,但二氧化硫的含量很少,没有将葡萄酒漂白,故选AC;
I.(2)1滴饱和亚硫酸溶液滴入3mL品红溶液中不褪色,而1滴品红溶液滴入3mL饱和亚硫酸溶液中褪色,说明二氧化硫或亚硫酸的含量会影响漂白效果,干白葡萄酒不能使品红溶液褪色,原因为:干白中二氧化硫或亚硫酸含量太少,故答案为:不合理,实验对比说明浓度低的亚硫酸不能使品红褪色,葡萄酒中的SO2含量很低,所以也不能使品红褪色;
Ⅱ.实验方案二:装置A中制备二氧化硫,X干燥二氧化硫,C中检验SO2与Na2O2反应是否有氧气,D中氢氧化钠溶液吸收剩余的二氧化硫,防止污染空气.E装置验证二氧化硫的还原性,F装置验证二氧化硫为酸性气体,并吸收二氧化硫,防止污染空气。
(3)关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没瓶中固体,A装置中亚硫酸钠与浓硫酸反应放出二氧化硫,二氧化硫被干燥后与过氧化钠反应生成硫酸钠,反应的方程式为SO2+Na2O2=Na2SO4,根据方程式,每消耗2molNa2O2,转移4mol电子,故答案为:SO2+Na2O2=Na2SO4;4NA;
(4)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F中,为了证明SO2有还原性,并从绿色化学的角度考虑,则Z试剂选择酸性KMnO4,高锰酸钾具有强氧化性,被二氧化硫还原褪色,发生反应的离子方程式为2MnO4— + 5SO2 +2 H2O = 2Mn2+ + 5SO42— + 4H+(或FeCl3溶液,SO2 +2 Fe3+ +2 H2O = 2 Fe 2+ + SO42— + 4H+);故答案为:酸性KMnO4;2MnO4— + 5SO2 +2 H2O = 2Mn2+ + 5SO42— + 4H+(或FeCl3溶液,SO2 +2 Fe3+ +2 H2O = 2 Fe 2+ + SO42— + 4H+);红色溶液变浅或褪色(或溶液由棕黄色变为浅绿色)。