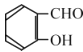
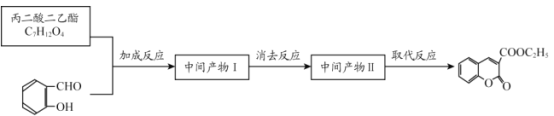
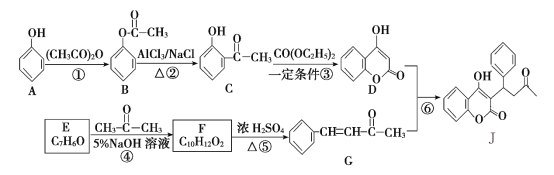
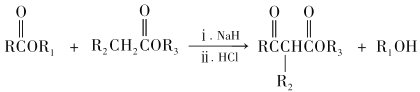��Ŀ����
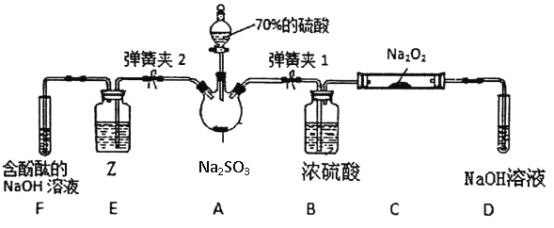
����Ŀ���軯��ұ������в��������ĺ����ˮ(��Ҫ����CN-��Cu(CN)32-��SO32-������)������ͨ����������������������д�����ijС��ͬѧ�Ըù��̽���ģ�⡣
����1����Һ�д���ƽ��Cu(CN)32-![]() CuCN��+2CN-
CuCN��+2CN-
����2��2Cu2++4CN-=2CuCN ��+(CN)2
(1)����CuCl2��Һ�Ժ����ˮ���г���������������Һ������(CNT)��������(CN-)��ȥ������CuCl2�������仯������ͼ��ʾ��

CuCl2������������(CNT)��������(CN-)ȥ���ʵ�Ӱ��
������ƽ���ƶ�ԭ�����ͣ�����CuCl2����������(3.0 g��ǰ)����Һ������(CNT)��������(CN-)��ȥ���ʱ仯����_________��
����SO32-�������£�CuCl2�ɽ���ˮ�е�Cu(CN)32-ֱ��ת��ΪCuCN�������ù��̵����ӷ���ʽΪ__________��
(2)�����ѵ缫�Գ�����ķ�Һ�в�����CN-�����ӽ�һ�����е�������һ���ĵ�ѹ�£��������۲쵽���Ե����ݣ������飬����Ҫ�ɷ�ΪN2��CO2����С��ͬѧʵ��ʱ���֣�����(1)�г�����CuCl2��ΪCuSO4����ⷨ��������ȥ��CN-��
�����й��ڵ��������������ˮ��˵����ȷ����__________��
A���������۲쵽��������Ҫ������ CN-�������ŵ������
B��������֮��С��ͬѧ���������ܻ��ս���ͭ
C����ⷨ���������У�Cu(CN)32-������Ǩ��
��CN-�а���̼����������������̼Ԫ�صĻ��ϼ�Ϊ ______��
�����û�ѧ�������͵�������Cl-�����ã�_________��
���𰸡���Һ��������������ȥ���ʾ���CuCl2�����������Ӷ����ӡ�������֪��Ϣ ii.�������ֱ�Ӻ�ͭ���ӷ�Ӧ��c(CN-)���ͣ�ƽ��Cu(CN)32-![]() CuCN��+ 2CN-�����ƶ���ʹ��Һ��Cu(CN)32-���ͣ��γ� CuCN ������ȥ�������ӡ� 2Cu2++Cu(CN)32-+SO32-+H2O=3CuCN��+2H+ +SO42- BC +2 ������2Cl--2e-=Cl2�������ɵ�Cl2��������Һ�е�CN-������N2��CO2��5Cl2 +2CN-+4H2O=10Cl- +2CO2��+ N2��+ 8H+���Ӷ�����Һ�е� CN-ȥ����
CuCN��+ 2CN-�����ƶ���ʹ��Һ��Cu(CN)32-���ͣ��γ� CuCN ������ȥ�������ӡ� 2Cu2++Cu(CN)32-+SO32-+H2O=3CuCN��+2H+ +SO42- BC +2 ������2Cl--2e-=Cl2�������ɵ�Cl2��������Һ�е�CN-������N2��CO2��5Cl2 +2CN-+4H2O=10Cl- +2CO2��+ N2��+ 8H+���Ӷ�����Һ�е� CN-ȥ����
��������
(1)�ٸ�����Һ������CuCl2����������(CNT)��������(CN-)ȥ������CuCl2�ı仯���Ʒ����жϣ�
��Cu2+��Cu(CN)32-��SO32-�ᷢ��������ԭ��Ӧ������ԭ���غ㡢�����غ�͵���غ㣬��д��Ӧ�����ӷ���ʽ��
(2)�ٵ��ʱ��������CN-ʧȥ���ӱ���������N2��CO2����Һ�������������������ƶ��������������������ƶ���
��CN-�а���̼������������C��NԪ�طǽ�����ǿ���жϸ�������̼Ԫ�صĻ��ϼۣ�
��Cl-�ڵ��ʱ����Cl2��Cl2���������ԣ�������CN-ΪN2��CO2��
(1)����ͼ���֪������CuCl2���룬��CuCl2������С��3.0 gǰ����Һ��������������ȥ���ʾ���CuCl2�����������Ӷ����ӣ��������ڸ�����Ϣ ii.�������ֱ�Ӻ�ͭ���ӷ�Ӧ��ʹ��Һ��c(CN-)���ͣ�����ƽ��ƽ��Cu(CN)32-![]() CuCN��+ 2CN-�����ƶ���ʹ��Һ��Cu(CN)32-���ͣ��γ�CuCN�������Ӷ�ʹȥ�������ӣ�
CuCN��+ 2CN-�����ƶ���ʹ��Һ��Cu(CN)32-���ͣ��γ�CuCN�������Ӷ�ʹȥ�������ӣ�
��Cu2+��Cu(CN)32-��SO32-�ᷢ��������ԭ��Ӧ����CuCN������SO42-������ԭ���غ㡢�����غ�͵���غ㣬�ɵø÷�Ӧ�����ӷ���ʽΪ��2Cu2++Cu(CN)32-+SO32-+H2O=3CuCN��+2H++SO42-��
(2)��A�������ѵ缫�Գ�����ķ�Һ�в�����CN- �����ӽ�һ�����е�������һ���ĵ�ѹ�£�������Cl-ʧȥ���ӱ�ΪCl2��Cl2��CN-��������N2��CO2����˿��������۲쵽���Ե����ݣ�A����
B������������Һ�е�Cu2+�õ����ӱ�ΪCu������������˵�����֮��С��ͬѧ���������ܻ��ս���ͭ��B��ȷ��
C�����ʱ����Һ�������������������ƶ���������Cu(CN)32-�������������ƶ���C��ȷ��
�ʺ���ѡ����BC��
��CN-�а���̼������������Ԫ�صķǽ�����C��N�����Թ��õ��Ӷ�ƫ��NԪ�أ�ʹCԪ����ʾ�����ϼۣ��������д�1����λ����ɣ�̼Ԫ�صĻ��ϼ���ֵΪ3-1=2������C���ϼ�Ϊ+2�ۣ�
����һ���ĵ�ѹ�£��������۲쵽���Ե����ݣ������飬����Ҫ�ɷ�ΪN2��CO2����С��ͬѧʵ��ʱ���֣�����(1)�г�����CuCl2��ΪCuSO4����ⷨ��������ȥ��CN-��˵���ڵ��ʱ������������Ӧ��2Cl--2e-=Cl2�������ɵ�Cl2��������Һ�е�CN-������N2��CO2�������˷�Ӧ5Cl2+2CN-+4H2O=10Cl-+2CO2��+ N2��+ 8H+���Ӷ�����Һ�е�CN-ȥ������SO42-����Һ�в���ʧȥ���ӣ���˵�ⷽ��ʹ��CuSO4����ⷨ��������ȥ��CN-��

 �������ͬ����ϰϵ�д�
�������ͬ����ϰϵ�д�����Ŀ��I.��1���������з�Ӧ��2SO2 + O2 ![]() 2SO3 �� ���2min��SO2��Ũ����8 mol/L�½�Ϊ2 mol/L����ô����SO2Ũ�ȱ仯����ʾ�Ļ�ѧ��Ӧ����Ϊ____����O2Ũ�ȱ仯����ʾ�ķ�Ӧ����Ϊ_____________�������ʼʱSO2Ũ��Ϊ4mol/L��2min��Ӧ��ƽ�⣬�����ʱ����v(O2)Ϊ0.5mol/(L��min)����ô2minʱSO2��Ũ��Ϊ_____________��
2SO3 �� ���2min��SO2��Ũ����8 mol/L�½�Ϊ2 mol/L����ô����SO2Ũ�ȱ仯����ʾ�Ļ�ѧ��Ӧ����Ϊ____����O2Ũ�ȱ仯����ʾ�ķ�Ӧ����Ϊ_____________�������ʼʱSO2Ũ��Ϊ4mol/L��2min��Ӧ��ƽ�⣬�����ʱ����v(O2)Ϊ0.5mol/(L��min)����ô2minʱSO2��Ũ��Ϊ_____________��
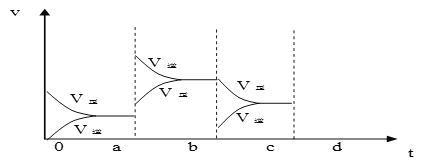
��2����ͼ��ʾ���ܱ������з�Ӧ��2SO2+O2![]() 2SO3 ��H<0 �ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯�����a b�����иı������������____________��b c�����иı������������____________�� ������ѹǿʱ����Ӧ�ٶȱ仯�������c-d��__________.
2SO3 ��H<0 �ﵽƽ��ʱ�����������ı������Ӧ�ٶȺͻ�ѧƽ��ı仯�����a b�����иı������������____________��b c�����иı������������____________�� ������ѹǿʱ����Ӧ�ٶȱ仯�������c-d��__________.
��3���������е���ƽ�⣺NH3��H2O![]() NH4+ + OH -����ʹc(NH4+)����Ĵ�ʩ�ǣ�_________
NH4+ + OH -����ʹc(NH4+)����Ĵ�ʩ�ǣ�_________
�������¶� �ڼӰ��� ��ˮ �� NH4Cl��Һ ��NaOH��Һ ������������
II.��һ��������ܱ������У��������»�ѧ��Ӧ��CO2��g����H2��g��![]() CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
CO��g����H2O��g�����仯ѧƽ�ⳣ��K���¶�t�Ĺ�ϵ���±���
t�� | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
�ش��������⣺
��1���÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��____________��
��2���÷�ӦΪ____________��Ӧ��ѡ�����ȡ����ȣ���
��3��ij�¶��£�ƽ��Ũ�ȷ�����ʽ��3c��CO2����c��H2����5c��CO����c��H2O�������жϴ�ʱ���¶�Ϊ____________�棻
��4��830��ʱ����������м���1LCO2��1LH2��ƽ��ʱCO2�����������____________��