题目内容
【题目】把1mol X气体和0.5mol Y气体混合于2L的密闭容器中,发生如下反应:
![]() ,2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,试计算
,2min末生成0.2mol W,若测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,试计算
(1)前2min内,用X表示的平均反应速率____________。
(2)前2min内Y的转化率____________。
(3)化学方程式中Z的化学计量数n____________。
【答案】0.075mol·L-1·min-1 20% 4
【解析】
2min末生成0.2mol W,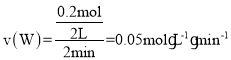 ,测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,由化学反应速率之比等于化学计量数之比可知,n=4,则反应方程式为:
,测得以Z的物质的量浓度变化表示的平均反应速率为0.1mol·L-1·min-1,由化学反应速率之比等于化学计量数之比可知,n=4,则反应方程式为:![]() ,据此可解答问题。
,据此可解答问题。
根据题干信息可建立三段式如下:
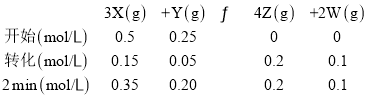
(1)前2min内,用X表示的平均反应速率![]() ,故答案为0.075mol·L-1·min-1;
,故答案为0.075mol·L-1·min-1;
(2)前2min内Y的转化率![]() ,故答案为:20%;
,故答案为:20%;
(3)根据以上分析可知可知n=4,故答案为:4。

练习册系列答案
相关题目